Nedre og Øvre Eksplosive Begrænsninger for Brændbare Gasser og Dampe


Hvad er %LEL / %UEL / PID
Før en brand-eller eksplosionsfare kan opstå, skal tre betingelser skal være opfyldt samtidigt.
a brændstof (dvs .. (luft) skal eksistere i visse proportioner sammen med en antændelseskilde, såsom en gnist eller flamme., Forholdet mellem brændstof og ilt, der kræves, varierer med hver brændbar gas eller damp.
den mindste koncentration af en bestemt brændbar gas eller damp, der er nødvendig for at understøtte dens forbrænding i luft, defineres som den nedre eksplosive grænse (Lel) for den gas. Under dette niveau er blandingen for “magert” til at brænde. Den maksimale koncentration af en gas eller damp, der brænder i luft, defineres som den øvre eksplosive grænse (UEL). Over dette niveau er blandingen for ” rig ” til at brænde. Området mellem LEL og UEL er kendt som det brændbare område for den gas eller damp.,
Metan – LEL: 5% af volumen i Luft / UEL: 17% af volumen i Luften
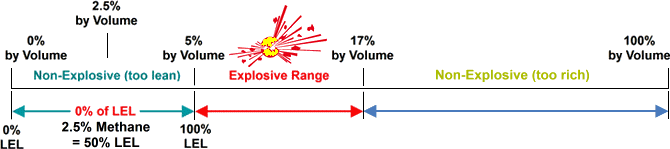
Visual eksempel for at vise, hvor på skalaen % af LEL måles
Nedre og Øvre Eksplosive Begrænsninger
De værdier, der vises i tabellen nedenfor er kun gældende for de forhold, under hvilke de blev bestemt (normalt stuetemperatur og atmosfærisk tryk ved hjælp af en 2 tommer rør med styret tænding). Brændbarhedsområdet for de fleste materialer udvides, når temperatur, tryk og beholderdiameter øges. Alle koncentrationer i volumenprocent.,
| Gas | LEL | UEL |
| Acetone | 2.6 | 13 |
| Acetylene | 2.5 | 100 |
| Acrylonitrile | 3 | 17 |
| Allene | 1.5 | 11.5 |
| Ammonia | 15 | 28 |
| Benzene | 1.3 | 7.9 |
| 1.3 Butadiene | 2 | 12 |
| Butane | 1.8 | 8.4 |
| n Butanol | 1.,7 | 12 |
| 1 Butene | 1.6 | 10 |
| Cis 2 Butene | 1.7 | 9.7 |
| Trans 2 Butene | 1.7 | 9.7 |
| Butyl Acetate | 1.4 | 8 |
| Carbon Monoxide | 12.5 | 74 |
| Carbonyl Sulfide | 12 | 29 |
| Chlorotrifluoro ethylene | 8.4 | 38.7 |
| Cumene | 0.9 | 6.5 |
| Cyanogen | 6.6 | 32 |
| Cyclohexane | 1.,3 | 7.8 |
| Cyclopropane | 2.4 | 10.4 |
| Deuterium | 4.9 | 75 |
| Diborane | 0.8 | 88 |
| Dichlorosilane | 4.1 | 98.8 |
| Diethylbenzene | 0.8 | |
| 1.1 Difluoro 1 Chloroethane | 9 | 14.8 |
| 1.1 Difluoroethane | 5.1 | 17.1 |
| 1.1 Difluoro ethylene | 5.5 | 21.3 |
| Dimethylamine | 2.8 | 14.,4 |
| Dimethyl Ether | 3.4 | 27 |
| 2.2 Dimethyl propane | 1.4 | 7.5 |
| Ethane | 3 | 12.4 |
| Ethanol | 3.3 | 19 |
| Ethyl Acetate | 2.2 | 11 |
| Ethyl Benzene | 1 | 6.7 |
| Ethyl Chloride | 3.8 | 15.4 |
| Ethylene | 2.7 | 36 |
| Ethylene Oxide | 3.6 | 100 |
| Gasoline | 1.2 | 7.,1 |
| Heptane | 1.1 | 6.7 |
| Hexane | 1.2 | 7.4 |
| Hydrogen | 4 | 75 |
| Hydrogen Cyanide | 5.6 | 40 |
| Hydrogen Sulfide | 4 | 44 |
| Isobutane | 1.8 | 8.4 |
| Isobutylene | 1.8 | 9.6 |
| Isopropanol | 2.2 | |
| Methane | 5 | 17 |
| Methanol | 6.,7 | 36 |
| Methylac etylene | 1.7 | 11.7 |
| Methyl Bromide | 10 | 15 |
| 3 Methyl 1 Butene | 1.5 | 9.1 |
| Methyl Cellosolve | 2.5 | 20 |
| Methyl Chloride | 7 | 17.4 |
| Methyl Ethyl Ketone | 1.9 | 10 |
| Methyl Mercaptan | 3.9 | 21.8 |
| Methyl Vinyl Ether | 2.6 | 39 |
| Monoethy lamine | 3.,5 | 14 |
| Monomethy lamine | 4.9 | 20.7 |
| Nickel Carbonyl | 2 | |
| Pentane | 1.4 | 7.8 |
| Picoline | 1.4 | |
| Propane | 2.1 | 9.5 |
| Propylene | 2.4 | 11 |
| Propylene Oxide | 2.8 | 37 |
| Styrene | 1.,1 | |
| Tetrafluoro ethylene | 4 | 43 |
| Tetrahydrofuran | 2 | |
| Toluene | 1.2 | 7.1 |
| Trichloro ethylene | 12 | 40 |
| Trimethylamine | 2 | 12 |
| Turpentine | 0.7 | |
| Vinyl Acetate | 2.6 | |
| Vinyl Bromide | 9 | 14 |
| Vinyl Chloride | 4 | 22 |
| Vinyl Fluoride | 2.6 | 21.,7 |
| Xylen | 1.1 | 6.6 |
| Gas | LEL | UEL |
Principper for Gas Detection
En af de mange krav, der for ind i lukkede rum, er måling til brændbare gasser. Før indtrængen af et begrænset rum skal niveauet af brandfarlige gasser være under 10% af LEL.
den mest almindelige sensor, der bruges til måling af LEL, er Wheheatstone bridge/catalytic bead / pellistor sensor (“Wheheatstone bridge”).,
Lel sensorer forklaret
en Wheheatstone bridge LEL sensor er simpelthen en lille elektrisk komfur med to brænderelementer. Et element har en katalysator (såsom platin) og man gør ikke ” t. begge elementer opvarmes til en temperatur, der normalt ikke ville understøtte forbrænding.
elementet med katalysatoren “brænder” gas på et lavt niveau og opvarmes i forhold til elementet uden katalysatoren. Det varmere element har mere modstand, og Wheheatstone bridge måler forskellen i modstand mellem de to elementer, som korrelerer med Lel.,

desværre fejler Wheheatstone bridge sensorer i en usikker tilstand; når de fejler, angiver de sikre niveauer af brændbare gasser. Svigt og / eller forgiftning af Wheheatstone bridge LEL sensor kan kun bestemmes gennem udfordrende Wheheatstone bridge sensorer med kalibrering gas.,
LEL-Sensorer Begrænsninger
To mekanismer, der påvirker udførelsen af Wheatstone bro LEL-sensorer og reducere deres effektivitet, når de anvendes for alle, men metan:
- Gasser brænde med forskellige varme udgange
Nogle gasser brænde varm og brænde nogle relativt køligt. Disse forskellige fysiske egenskaber fører til vanskeligheder ved brug af Lel-sensorer. For eksempel brænder 100% Lel-methan (5% methan efter volumen) med to gange varmen af 100% Lel-propan (2, 0 propan efter volumen)., - Tungere kulbrinter dampe har svært ved at diffundere ind LEL-sensorer og reducere deres output
Nogle af de Tungere kulbrinter dampe har svært ved at diffundere gennem sintret metal flamme han på LEL-sensorer. Denne flammeangreb er nødvendig for at forhindre selve sensoren i at starte en brand og forhindrer ikke gasser som methan, propan og Ethan i at nå Wheheatstone-broen. Imidlertid diffunderer kulbrinter som Ben .in, diesel, opløsningsmidler osv.langsommere gennem flammeangreb, så mindre damp når Wheheatstone-broen, og sensoren giver mindre output.,
hvorfor ikke bruge en Lel-skærm?
mange flygtige organiske forbindelser (VOC ‘ er) er brandfarlige og kan detekteres af Lel-eller brændbare gassensorer, der findes i stort set alle multigas-skærme. Lel-sensorer er imidlertid ikke særlig nyttige til måling af toksicitet, fordi de ikke har tilstrækkelig følsomhed.
Hvad er nogle almindelige VOC ‘ er?,
Voc er den kemiske forbindelser at holde industrien i gang og er:
- Brændstoffer
- Olier, °reasers, varmetransporterende Væsker
- Opløsningsmidler, Maling
- Plast, Resin og deres forstadier
- og mange andre
Voc ‘ er, der findes i hele branchen, fra den indlysende applikationer i den petro-kemiske industri til ikke-så-indlysende applikationer såsom pølse produktion.

hvad menes med PPM?
Parts per million (ppm) er en almindeligt anvendt koncentrationsenhed for små værdier., En del pr million er en del af opløst stof pr million dele opløsningsmiddel eller 10-6. Dele pr million og andre” dele pr ” notationer (f.dele pr milliard eller dele pr Billion) er dimensionsløse mængder uden enheder. Foretrukne metoder til at udtrykke dele per million omfatter µV/V (microvolume per volumen), µL/L (microliters per liter), mg/kg (milligram per kilo), μ mol/mol (mikromol per mol), og µm/m (mikrometer pr meter).,”notationen bruges til at beskrive fortyndede opløsninger inden for Kemi og teknik, men dens betydning er tvetydig, og den er ikke en del af SI-målesystemet. Årsagen til, at systemet er tvetydigt, er, at koncentrationen afhænger af den originale enhedsfraktion, der bruges. For eksempel er sammenligning af en milliliter af en prøve til en million milliliter forskellig fra at sammenligne en mol til en million mol eller et gram til en million gram.
University of Minnesota giver nogle andre analogier, der kan hjælpe dig med at visualisere skalaen involveret i PPM.,
En ppm er ligesom:
- en tomme i 16 km
- en anden i 11.5 dage
- et minut i to år
- en bil i kofanger til kofanger trafik fra Cleveland til San Francisco
Andre visualisering af skalaen, der er involveret med PPB
En PPB er ligesom:
- tilføje en knivspids salt til en 10 ton pose chips
- En ppb er som et ark i en rulle toiletpapir, der strækker sig fra New York til London.,
LEL-sensorer måler eksplosivitet, ikke toksicitet
LEL-sensorer måler procent af Lel. For eksempel har Ben .in en Lel på 1,4%. Derfor 100% af LEL er 14.000 ppm af benzin, 10% af LEL er 1.400 ppm af benzin og 1% af LEL er 140 ppm af benzin.140 ppm ben .in er den laveste mængde damp, som Lel-skærmen kan “se.”Ben .in har en T .a på 300 ppm og en STEL på 500 ppm; dette gør ikke Lel-sensorer velegnede til måling af ben .indampe, fordi de simpelthen ikke giver tilstrækkelig opløsning.Lel-sensorer måler eksplosivitet, ikke toksicitet., Mange VOC ‘ er er potentielt giftige på niveauer, der ligger langt under deres eksplosive niveauer og under Lel-sensorernes følsomhed.
som beskrevet ovenfor:
et af de mange krav til adgang til lukkede rum kaldet er måling af lukkede rum for brandfarlige gasser.
før indtræden af et begrænset rum skal niveauet af brændbare gasser være under 10% af LEL.
den mest almindelige sensor, der bruges til måling af LEL, er Wheheatstone bridge/catalytic bead / pellistor sensor (“Wheheatstone bridge”).,
mens det er nyttigt i en lang række applikationer, har Wheheatstone bridge Lel-sensorer enten ikke tilstrækkelig følsomhed over for et bestemt kemikalie, eller kemikalier, der anvendes i miljøet, kan gøre Wheheatstone bridge-sensoren ubrugelig.
under disse typer omstændigheder kan PID ‘ er (fotoioniseringsdetektorer) give et alternativt, meget nøjagtigt og giftfrit middel til måling af 10% af LEL til begrænset plads.

Hvad er en PID?,
en Fotoioniseringsdetektor måler VOC ‘ er og andre giftige gasser i lave koncentrationer fra ppb (dele pr.milliard) op til 10.000 ppm (dele pr. million eller 1 volumenprocent).
en PID er en meget følsom bredspektret skærm, som en “LEL-skærm på lavt niveau. En Fotoioniseringsdetektor måler VOC ‘ er og andre giftige gasser i lave koncentrationer fra ppb (parts per billion) op til 10.000 ppm (parts per million eller 1 volumenprocent). En PID er en meget følsom bredspektret skærm, som en “Lel-skærm på lavt niveau.
Hvordan virker en PID?,
en Fotoioniseringsdetektor (PID) bruger en Ultraviolet (UV) lyskilde (foto= lys) til at nedbryde kemikalier til positive og negative ioner (ionisering), der let kan tælles med en detektor. Ionisering opstår, når et molekyle absorberer UV-lyset med høj energi, hvilket ophidser molekylet og resulterer i midlertidigt tab af en negativt ladet elektron og dannelsen af positivt ladet ion.
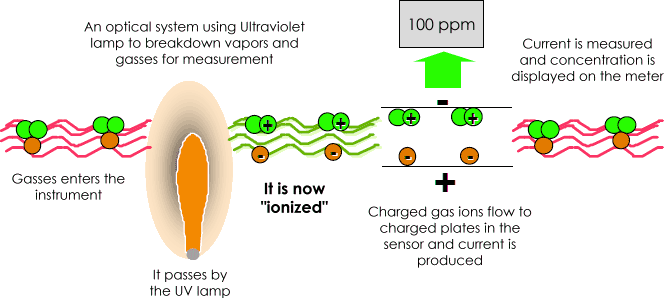
gassen bliver elektrisk ladet., I detektoren producerer disse ladede partikler en strøm, der derefter forstærkes og vises på måleren som “ppm” (dele pr.
ionerne rekombineres hurtigt efter elektroderne i detektoren for at “reformere” deres oprindelige molekyle.
PID ‘ er er ikke-destruktive; de “brænder” ikke eller ændrer prøvegassen permanent, hvilket gør det muligt for dem at blive brugt til prøvetagning.
hvad måler en PID?
den største gruppe af forbindelser målt ved en PID er de organiske stoffer: forbindelser indeholdende Carbon (C) atomer.,s containing a benzene ring including benzene, toluene, ethyl benzene and xylene