Tungt vand
tungt vand er vand, der indeholder tungt brint – også kendt som deuterium – i stedet for almindeligt brint. Det kan også være skrevet som 2H2O eller D2O. Deuterium er anderledes end den brint, der normalt forekommer i vand—kendt som protium, da hvert atom af deuterium indeholder en proton og en neutron, mens de mere almindeligt forekommende brint indeholder kun en proton.
tungt vand forekommer naturligt, dog i meget mindre mængder end almindeligt vand., CA. et vandmolekyle for hver tyve millioner vandmolekyler er tungt vand. Da deuterium er en stabil isotop, er tungt vand ikke radioaktivt.
ud over at være nyttigt til atomreaktorer er tungt vand også blevet brugt i Canada til at detektere neutrinoer fra solen på Sudbury Neutrino Observatory, hvilket giver vigtig indsigt i subatomisk fysik.
anvendelse som Moderator
hovedside
i nukleare fissionsreaktorer skal neutronerne Sænkes for at sikre, at der opstår en effektiv fissionskædereaktion., Denne proces med at bremse neutroner ned er kendt som moderation, og det materiale, der bremser disse neutroner, er kendt som en neutron moderator. Tungt vand er en af de to moderatorer, der kan bruges, som tillader en atomreaktor at fungere ved hjælp af naturligt uran. Den anden moderator er graphite.
en tungvandsreaktor bruger tungt vand som kølevæske og moderator. Deuterium fungerer som moderator, da det absorberer færre neutroner end brint, hvilket er ekstremt vigtigt, da nukleare fissionsreaktioner kræver neutroner til at udføre deres kædereaktioner., Det tunge vand holdes under tryk, hvilket øger kogepunktet, så det kan fungere ved høje temperaturer uden kogning. CANDU reaktorer udnytte tungt vand som deres moderator og dermed ikke kræver beriget uran, snarere uran i sin naturlige tilstand kan anvendes.
Produktion
udgifterne til det tunge vand er en væsentlig del af byggeomkostningerne for en tungvandsreaktor, men gør reaktorerne billigere at betjene (da uranberigelse ikke er nødvendig). Teknisk set er deuterium ikke “lavet” i en bestemt proces, snarere adskilles molekyler af tungt vand fra store mængder vand indeholdende H2O eller enkeltvis deutereret vand i Girdler sulfidprocessen (som vil blive diskuteret i detaljer i de næste to afsnit). Vandet, der ikke er tungt, kasseres og kaldes “udtømt vand”., En alternativ metode findes, når vand elektrolyseres for at fremstille ilt og brint, der indeholder normal gas, sammen med deuterium. Brintet bliver derefter flydende og destilleret for at adskille de to komponenter, så omsættes deuteriet med ilt for at danne tungt vand. produktion af tungt vand kræver avanceret infrastruktur, og tungt vand produceres aktivt i Argentina, Canada, Indien og Norge. Den største fabrik var Bruce-anlægget i Canada, men har lukket ned., Teknisk set er der en lille forskel i kogepunkterne for tungt vand og vand, så denne forskel kunne udnyttes ved ekstraktion af tungt vand. Imidlertid, da deuterium findes i så lille antal, ville en enorm mængde vand være nødvendigt at koge for at opnå betydelige mængder deuterium. Dette ville kræve meget brændstof eller elektricitet, så i stedet udnytter faciliteter kemiske forskelle mellem de to. Den vigtigste kemiske metode til fremstilling af tungt vand er Girdler sulfidprocessen.,
Girdler sulfidprocessen er en metode, der virker baseret på en udveksling af deuterium mellem H2S og almindeligt let vand. I denne proces er der to separate kolonner. Den ene kolonne er ved 30.C og er kendt som “cold to .er”, mens den anden er ved 130. C, kendt som “hot to .er”. Adskillelsen sker baseret på en ligevægt og forskellene i ligevægt ved de to forskellige temperaturer. Ligevægtsligningen er:
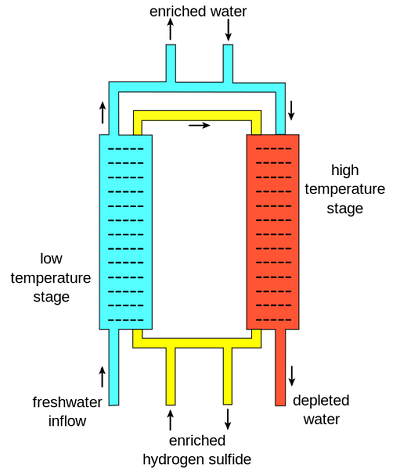
hovedårsagen til, at denne proces fungerer, er et resultat af, at hydrogensulfidgas cirkuleres mellem varme og kolde tårne., Først strømmer ferskvand ind i lavtemperaturtrinnet sammen med deuteriumberiget hydrogensulfidgas. Som et resultat af ligevægtsegenskaberne ved denne temperatur migrerer deuterium fortrinsvis fra det berigede hydrogensulfid til vandet, hvilket skaber tungt vand. Dette berigede vand tages derefter af, og mere ferskvand kommer ind i høj temperaturstadiet sammen med hydrogensulfidgassen (nu lidt udtømt i deuterium). Her bevæger ethvert deuterium fra ferskvand fortrinsvis til hydrogensulfidgassen og beriger det., Denne berigede gas bevæger sig derefter tilbage til lavtemperaturstadiet og arbejder for yderligere at berige det tunge vand. Normalt vand fra høj temperaturstadiet, nu udtømt, trækkes af. Derefter opstilles en kaskade, så” beriget ” vand—vand med mere deuterium— føres ind i det kolde tårn og beriges igen.