Diclofenaco
Diclofenaco
Solución inyectable y grageas de liberación prolongada
Analgésico, antiinflamatorio,
antirreumático
FORMA FARMACÉUTICA Y FORMULACIÓN:
Cada ampolleta contiene:
Diclofenaco sódico……………………………………………………. 75 mg
Agua inyectable, 3 ml.
Cada GRAGEA de liberación prolongada contiene:
Diclofenaco sódico………………………………………………….., 100 mg
INDICACIONES TERAPÉUTICAS: DICLOFENACO sódico es un antiinflamatorio que posee actividades analgésicas y antipiréticas y está indicado por vía oral e intramuscular para el tratamiento de enfermedades reumáticas agudas, artritis reumatoidea, espondilitis anquilosante, artrosis, lumbalgia, gota en fase aguda, inflamación postraumática y postoperatoria, cólico renal y biliar, migraña aguda, y como profilaxis para dolor postoperatorio y dismenorrea.,
CONTRAINDICACIONES: DICLOFENACO sódico está contraindicado en presencia de úlcera gástrica o intestinal, hipersensibilidad conocida a la sustancia activa, al metabisulfito y a otros excipientes.
Está contraindicado en pacientes que han tenido asma, urticaria o rinitis aguda después de la administración de ácido acetilsalicílico u otros medicamentos que inhiben la prostaglandina sintetasa. En presencia de hipertensión arterial severa, insuficiencia cardiaca, renal y hepática, citopenias.,
PRECAUCIONES GENERALES: Los efectos en vía gastrointestinal son los más habituales cuando se utiliza la vía oral. Se observa hemorragia, úlcera o perforación de la pared intestinal.
Se debe tener cuidado en pacientes con insuficiencia hepática y renal. Después de la ingesta crónica por más de 8 semanas, hay que evaluar los efectos de la aminotransferasa e interrumpir el fármaco si hay cifras anormales de la aminotransferasa.,
RESTRICCIONES DE USO DURANTE EL EMBARAZO Y LA LACTANCIA:
Categoría de riesgo B: Hasta el presente, son insuficientes los datos disponibles acerca del empleo de DICLOFENACO durante el embarazo y la lactancia, por ello, no se recomienda durante el embarazo y la lactancia.
REACCIONES SECUNDARIAS Y ADVERSAS: En términos generales se consideran reacciones adversas frecuentes cuando su incidencia es mayor de 10%, ocasionales entre 1 a 10%; reacciones adversas entre 0.001 a 1%, en casos aislados menos de 0.001%.,
Las reacciones adversas se mencionan de acuerdo con el sitio de afección.
Tracto gastrointestinal: Dolor epigástrico, otros trastornos gastrointestinales como náusea, vómito, diarrea, calambres abdominales, dispepsia, flatulencia y anorexia. Raras veces: hemorragias gastrointestinales (hematemesis, melena, diarrea sanguinolenta), úlcera gástrica o intestinal con o sin hemorragia o perforación., Casos aislados: estomatitis aftosa, glositis, lesiones esofágicas, estenosis intestinales por deformación de «diafragmas”, trastornos intestinales bajos como colitis hemorrágica inespecífica y exacerbación de la colitis ulcerosa o enfermedad de Crohn, estreñimiento y pancreatitis.
Sistema nervioso central: En ocasiones: cefalea, mareo o vértigo. Rara vez: somnolencia., Casos aislados: trastornos de la sensibilidad, inclusive parestesias, trastornos de la memoria, desorientación, insomnio, irritabilidad, convulsiones, depresión, ansiedad, pesadillas, temblor, reacciones psicóticas, meningitis aséptica.
Sentidos especiales: Casos aislados: trastornos de la visión (visión borrosa, diplopía), pérdida de la audición, tinnitus, alteraciones del gusto.
Piel: En ocasiones: eritemas o erupciones cutáneas. Rara vez: urticaria., Casos aislados: erupciones bulosas, eccemas, eritema multiforme, síndrome de Stevens-Johnson, síndrome de Lyell (epidermólisis tóxica aguda), eritrodermia (dermatitis exfoliativa), caída del cabello, reacción de fotosensibilidad; púrpura, inclusive púrpura alérgica.
Hematológicas: Casos aislados: trombocitopenia, leucopenia, anemia (hemolítica, aplásica), agranulocitosis.
Riñones: Casos aislados: insuficiencia renal aguda, alteraciones urinarias como hematuria, proteinuria, nefritis intersticial, síndrome nefrótico y necrosis papilar.,
Hígado: En ocasiones: aumento de los valores séricos de aminotransferasas. Rara vez: hepatitis con o sin ictericia. Casos aislados: hepatitis fulminante.
Hipersensibilidad: Rara vez: reacciones de hipersensibilidad como asma, reacciones sistémicas anafilácticas/anafilactoides, inclusive hipotensión. Casos aislados: vasculitis, neumonitis.
Sistema cardiovascular: Casos aislados: palpitación, dolor torácico, hipertensión e insuficiencia cardiaca congestiva.,
Otros sistemas orgánicos: Ocasionales: reacciones en el punto de la inyección intramuscular como dolor local y endurecimiento. Casos aislados: abscesos locales y necrosis en el punto de la inyección intramuscular.
INTERACCIONES MEDICAMENTOSAS Y DE OTRO GÉNERO: La administración concomitante de DICLOFENACO sódico y agentes preparados a base de litio o digoxina puede elevar el nivel plasmático de éstos.
Es posible que diversos agentes antiinflamatorios no esteroideos inhiban el efecto de los diuréticos.,
Puede ser que el tratamiento concomitante con diuréticos que ahorran potasio esté relacionado con una hiperpotasemia, lo que obliga a vigilar los niveles séricos del potasio. La administración concomitante con antiinflamatorios sistémicos no esteroideos puede favorecer la aparición de efectos colaterales.
En estudios clínicos, parece que DICLOFENACO sódico no influye sobre el efecto de los antiinflamatorios; sin embargo, existen reportes de que aumenta el peligro de hemorragia con un empleo combinado con anticoagulantes.,
En estudios clínicos se ha demostrado que DICLOFENACO sódico se puede administrar de manera concomitante con antidiabéticos orales sin que se altere el efecto clínico. Sin embargo, se han reportado algunos casos en que se producen tanto hipo como hiperglucémicos con DICLOFENACO sódico, por lo que se requiere modificar la dosificación del hipoglucemiante.,
Con la administración de metotrexato se debe tener precaución cuando se empleen los antiinflamatorios no esteroideos en periodos menores de 24 horas antes o después del tratamiento, ya que se puede elevar la concentración sanguínea del metotrexato y con ello aumentar su toxicidad. Los efectos de los AINEs sobre las prostaglandinas pueden aumentar la nefrotoxicidad de la ciclosporina.
Existen informes aislados de convulsiones debidas posiblemente al empleo concomitante de quinolonas y antiinflamatorios no esteroideos.,
PRECAUCIONES EN RELACIÓN CON EFECTOS DE CARCINOGÉNESIS, MUTAGÉNESIS, TERATOGÉNESIS Y SOBRE LA FERTILIDAD: En estudios en ratas de experimentación, se determinó que DICLOFENACO no influyó en la fertilidad de los animales progenitores, así como tampoco en el desarrollo pre, peri y posnatal de la descendencia.
En estudios en animales de experimentación no se detectaron efectos teratogénicos. En experimentos tanto in vitro como in vivo, en estudios prolongados con ratas y ratones tampoco se ha podido demostrar efectos mutagénicos ni potencial carcinogénico.,
DOSIS Y VÍA DE ADMINISTRACIÓN:
Oral, intramuscular e intravenosa por infusión.
La dosis oral va de 100 a 200 mg diariamente.
Adultos: Sólo aplicar las ampolletas durante dos días, y en caso necesario, se puede proseguir con grageas de DICLOFENACO.
Intramuscular: En general, la dosis es una ampolleta diaria de 75 mg por vía intraglútea profunda en el cuadrante superior externo. Sólo de manera excepcional, en casos graves se pueden administrar dos inyecciones diarias de 75 mg con un intervalo de varias horas.,
En los ataques de migraña, el empleo inicial es de una ampolleta de 75 mg administrada lo antes posible. La dosis total no deberá exceder de 175 mg el primer día.
Niños: La administración intravenosa se lleva a cabo mediante infusión lenta. Para el tratamiento del dolor postoperatorio de moderado a severo, infundir 75 mg en forma continua en un periodo de 30 minutos a dos horas. Si es necesario, puede retirarse después de pocas horas, pero la dosis no debe exceder de 150 mg en 24 horas.,
Para la prevención de dolor postoperatorio, administrar por infusión 25 a 50 mg después de la cirugía, en un periodo de 15 minutos a 1 hora, seguidos de una infusión continua de aproximadamente 5 mg por hora, hasta una dosis máxi-
ma de 150 mg en 24 horas.
Las infusiones intravenosas deberán realizarse inmediatamente después de preparar las soluciones para la infusión. No deberán conservarse las soluciones preparadas para infusión. Sólo se deben usar soluciones claras; si se observan cristales o precipitación de la solución, no se debe administrar la infusión., La solución inyectable de DICLOFENACO sódico no se debe administrar por infusión intravenosa en bolo. No se recomienda la administración de DICLOFENACO Solución Inyectable en niños.
MANIFESTACIONES Y MANEJO DE LA SOBREDOSIFICACIÓN O INGESTA ACCIDENTAL: El tratamiento de la intoxicación aguda con antiinflamatorios no esteroideos consiste en medidas de apoyo y sintomáticas. No se conoce un cuadro clínico típico tras la sobredosificación con DICLOFENACO.,
Medidas terapéuticas en caso de sobredosis: Medidas de apoyo y sintomáticas contra complicaciones como hipotensión, insuficiencia renal, convulsiones, irritación gastrointestinal y depresión respiratoria. Los tratamientos específicos como diuresis forzada, diálisis o hemoperfusión, son probablemente poco útiles para eliminar los antiinflamatorios no esteroideos a causa de su elevada tasa de fijación proteica y su metabolismo extenso.
RECOMENDACIONES SOBRE ALMACENAMIENTO:
Consérvese a temperatura ambiente a no más de 30°C y en lugar seco.,
LEYENDAS DE PROTECCIÓN:
Literatura exclusiva para médicos. Su venta requiere
receta médica. No se deje al alcance de los niños. No se administre
durante el embarazo, en la lactancia ni en niños menores de 12 años.
NOMBRE Y DOMICILIO DEL LABORATORIO:
Véase Presentación o Presentaciones.
PRESENTACIÓN O PRESENTACIONES:
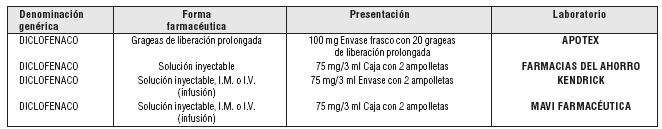

Fuente: S.S.A. Catálogo de Medicamentos Genéricos Intercambiables para farmacias y público en general al 3 de agosto de 2007.,
Con el objeto de demostrar la intercambiabilidad a que se refiere el artículo 75 del reglamento de Insumos para la Salud, los medicamentos que integran
el Catálogo de Medicamentos Genéricos Intercambiables han sido comparados, siguiendo los lineamientos indicados por la NOM-177SSA1-1998,
contra los productos innovadores o de referencia enlistados en las págs. 11 a 22 donde usted lo podrá consultar.