10.6: Rácsos Szerkezetek, Kristályos, Szilárd anyag
Egység Sejtek Fémek
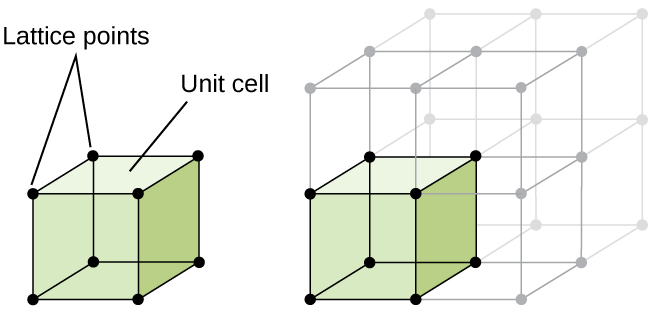
A szerkezet egy kristályos, szilárd anyag, akár fém, akár nem, a legjobb által leírt tekintve a legegyszerűbb ismétlődő egység, amely a továbbiakban az elemi cella. Az egységcella rácspontokból áll, amelyek az atomok vagy ionok helyét képviselik. Az egész szerkezet ezután három dimenzióban ismétlődő egységcellából áll, amint azt a \(\PageIndex{1}\) ábra szemlélteti.,
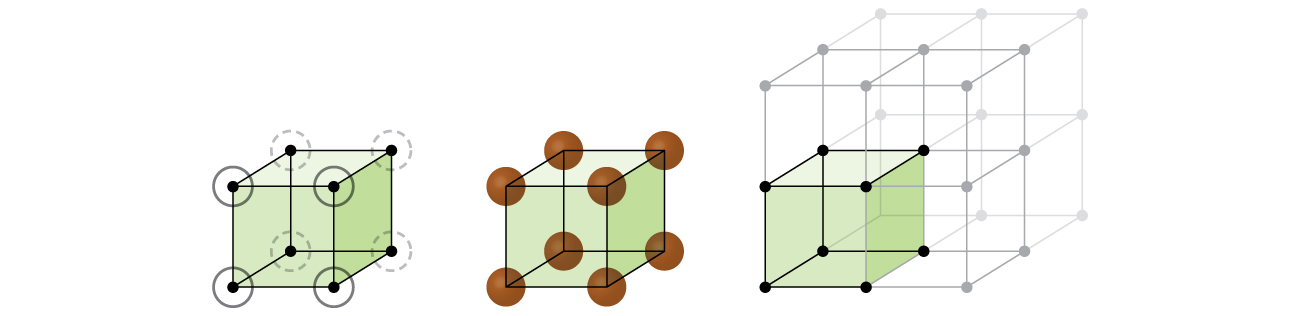
kezdjük el a kristályrácsszerkezet és az egységcellák vizsgálatát a legegyszerűbb szerkezettel és a legalapvetőbb egységcellával. Ennek megjelenítéséhez képzelje el, hogy nagyszámú azonos gömböt, például teniszlabdát vesz fel, és egyenletesen rendezi őket egy tartályba., Ennek legegyszerűbb módja az lenne, ha olyan rétegeket hoznánk létre, amelyekben az egyik rétegben lévő gömbök közvetlenül az alábbi rétegben vannak, amint azt a \(\PageIndex{2}\) ábra szemlélteti. Ezt az elrendezést Egyszerű köbös szerkezetnek nevezik, az egységcellát pedig egyszerű köbös egységcellának vagy primitív köbös egységcellának nevezik.
egy egyszerű köbös szerkezetben a gömbök nincsenek olyan szorosan csomagolva, amennyire csak lehet, és csak a tartály térfogatának 52% – át töltik ki. Ez egy viszonylag nem hatékony elrendezés, csak egy fém (polónium, Po) kristályosodik egy egyszerű köbös szerkezetben. Amint az a \(\PageIndex{3}\) ábrán látható, egy ilyen típusú elrendezésű szilárd anyag síkokból (vagy rétegekből) áll, amelyekben minden atom csak a réteg négy legközelebbi szomszédjával érintkezik; egy atom közvetlenül felette a fenti rétegben; és egy atom közvetlenül alatta az alábbi rétegben., Az egyéb részecskék számát, amelyeket minden részecske kristályos szilárd érintkezésben ismer, koordinációs számának nevezik. Egy egyszerű köbös tömbben lévő polónium atom esetében a koordinációs szám tehát hat.

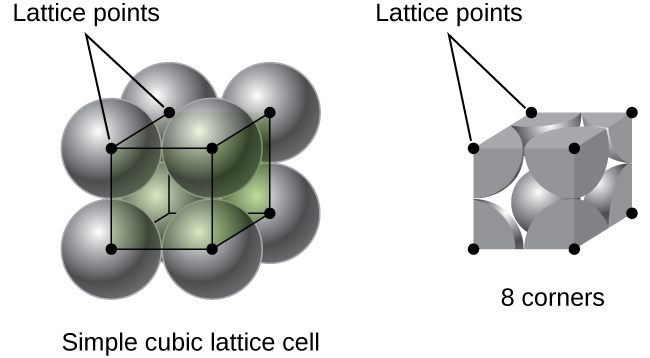
egy egyszerű köbös rácsban az egységcella, amely minden irányban megismétlődik, egy kocka, amelyet nyolc Atom középpontjai határoznak meg, amint azt a \(\PageIndex{4}\) ábra mutatja. Az egységcella szomszédos sarkaiban lévő atomok érintkeznek egymással, így ennek a cellának a szélhossza megegyezik két atomi sugárral vagy egy atomi átmérővel. A köbös egységcella csak ezen atomok azon részeit tartalmazza, amelyek benne vannak. Mivel egy egyszerű köbös egységcella sarkában lévő atomot összesen nyolc egységcella tartalmaz, ennek az atomnak csak egynyolcada van egy adott egységcellán belül., Mivel minden egyszerű köbös egységcellának van egy atomja a nyolc “sarkán”, van \(8× \ dfrac{1}{8}=1\) atom egy egyszerű köbös egységcellán belül.
a legtöbb fémkristály az egységcellák négy fő típusának egyike., Most a három köbös egységcellára összpontosítunk: egyszerű köbös (amit már láttunk), testközpontú köbös egységcellára, valamint arcközpontú köbös egységcellára-amelyek mindegyikét a \ábra szemlélteti(\PageIndex{5}\). (Vegye figyelembe, hogy valójában hét különböző rácsrendszer létezik, amelyek közül néhány egynél több típusú rácsot tartalmaz, összesen 14 különböző típusú egységcellára. A bonyolultabb geometriákat később hagyjuk ebben a modulban.,)
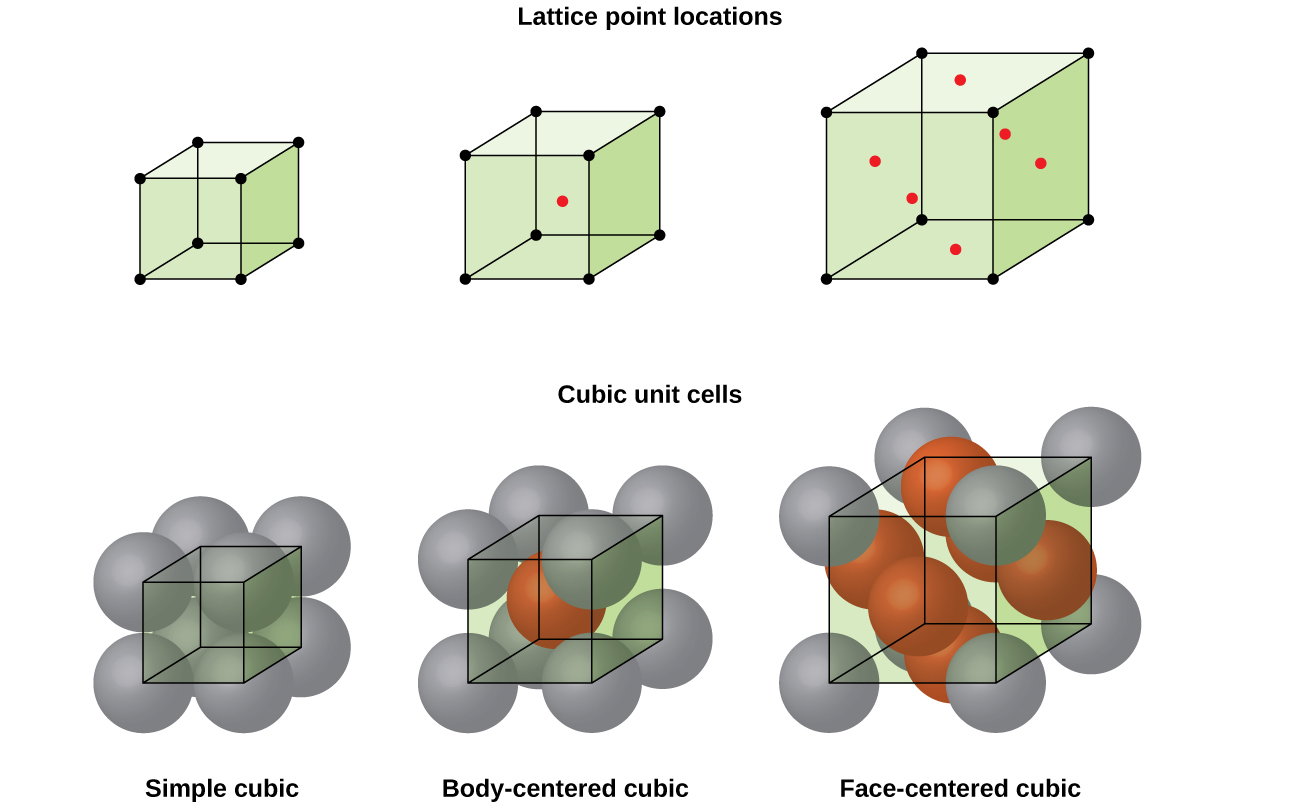
egyes fémek olyan elrendezésben kristályosodnak ki, amelynek köbös egységcellája van atomokkal az összes sarkon, és egy atom a közepén, amint azt a \(\PageIndex{6}\) ábra mutatja. Ezt testközpontú köbös (BCC) szilárdnak nevezik., A BCC egységcellák sarkaiban lévő atomok nem érintkeznek egymással, hanem érintkeznek a központban lévő atommal. A BCC egységcellája két atomot tartalmaz: az atom egynyolcadát a nyolc sarok mindegyikén (\(8× \ dfrac{1}{8}=1\) atom a sarkokból) plusz egy atom a központból. Bármely atom ebben a struktúrában négy atomot érint a felette lévő rétegben, négy atomot pedig az alatta lévő rétegben. Így egy atom egy BCC struktúrában nyolc koordinációs számmal rendelkezik.,
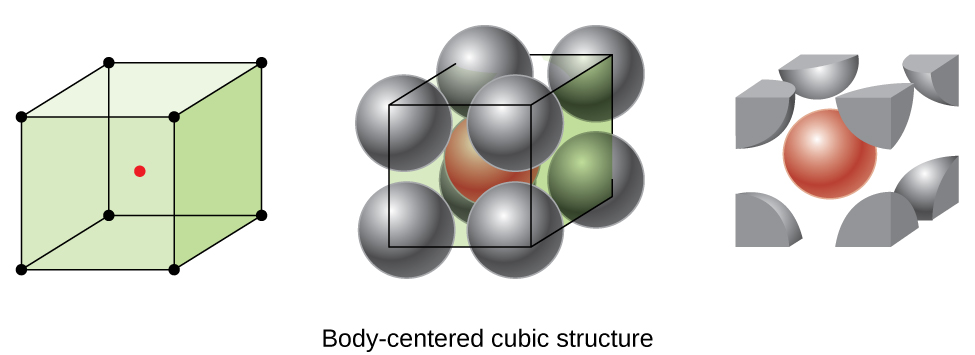
a BCC elrendezésekben lévő atomok sokkal hatékonyabban vannak csomagolva, mint egy egyszerű köbös szerkezetben, amely a teljes térfogat körülbelül 68% – át foglalja el. A BCC szerkezetű izomorf fémek közé tartozik a K, Ba, Cr, Mo, W és FE szobahőmérsékleten., (Az azonos szerkezetű kristályosodó elemeket vagy vegyületeket izomorfnak mondják.)
sok más fém, mint például az alumínium, a réz és az ólom, olyan elrendezésben kristályosodik, amelynek köbös egységcellája van atomokkal minden sarkon és az egyes arcok közepén, amint azt a \(\PageIndex{7}\) ábra szemlélteti. Ezt az elrendezést arc-központú köbös (FCC) szilárdnak nevezik., Egy FCC egység sejt tartalmaz négy atom: egy-nyolcadik egy atom mind a nyolc sarkok (\(8×\dfrac{1}{8}=1\) atom a sarkok), a másik fele egy atom mind a hat arcok (\(6×\dfrac{1}{2}=3\) az atomok az arcok). A sarkokban lévő atomok érintik az atomokat a szomszédos arcok közepén a kocka átlói mentén. Mivel az atomok azonos rácspontokon vannak, azonos környezetük van.
Az FCC elrendezésben lévő atomok a lehető legszorosabban össze vannak csomagolva, az atomok a térfogat 74% – át foglalják el., Ezt a szerkezetet köbös legközelebbi csomagolásnak (CCP) is nevezik. A CCP-ben három ismétlődő réteg hatszögletű elrendezésű atom van. Minden atom hat atomot érint a saját rétegében, három a fenti rétegben, három pedig az alábbi rétegben. Ebben az elrendezésben minden atom 12 szomszédhoz ér, ezért 12 koordinációs számmal rendelkezik. Az a tény, hogy az FCC és a CCP-megállapodások egyenértékűek, nem feltétlenül nyilvánvaló, de miért valójában ugyanaz a szerkezet, a \(\PageIndex{8}\) ábrán látható.,
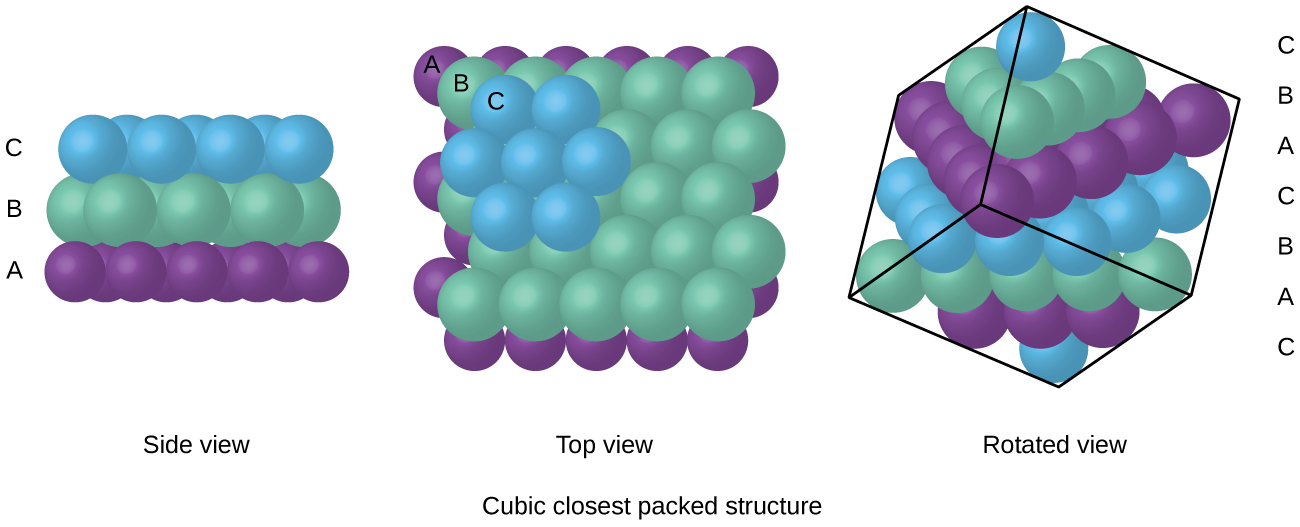
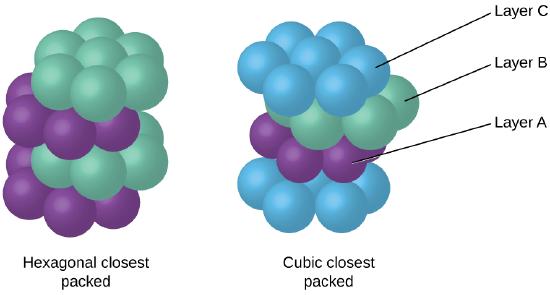
mivel a szorosabb csomagolás maximalizálja az atomok közötti általános vonzerőt, és minimalizálja a teljes intermolekuláris energiát, a legtöbb fémben lévő atomok ilyen módon csomagolnak., Az egyszerű fémkristályos szerkezetekben kétféle legközelebbi csomagolást találunk: a CCP-t, amellyel már találkoztunk, valamint a hatszögletű legközelebbi csomagolást (HCP), amely a \(\PageIndex{9}\) ábrán látható. Mindkettő hatszögletű elrendezésű atomok ismétlődő rétegeiből áll. Mindkét típusban egy második réteget (B) helyeznek az első rétegre (A) úgy, hogy a második réteg minden atomja érintkezzen az első réteg három atomjával. A harmadik réteg kétféleképpen helyezkedik el. A HCP-ben a harmadik réteg atomjai közvetlenül az első réteg atomjai felett vannak (azaz,, a harmadik réteg szintén a típus), a halmozás pedig váltakozó a típusú és B típusú zárt rétegekből áll (azaz ABABAB⋯). A CCP-ben a harmadik réteg atomjai az első két réteg egyikében sem állnak az atomok felett (azaz a harmadik réteg C típusú), a halmozás pedig váltakozó a típusú, B típusú és C típusú zárt rétegekből áll (azaz ABCABCABC⋯). Az összes fém körülbelül kétharmada kristályosodik a legközelebb csomagolt tömbökben, 12 koordinációs számmal., A HCP szerkezetében kristályosodó fémek közé tartozik a Cd, Co, Li, Mg, Na és Zn, és a CCP szerkezetben kristályosodó fémek közé tartozik az Ag, Al, Ca, Cu, Ni, Pb és Pt.
Exercise \(\PageIndex{2}\)
Az ezüst FCC szerkezetben kristályosodik. Az egységcellájának élhossza 409 pm.
- mi az AG atomi sugara ebben a struktúrában?
- Számítsa ki az Ag sűrűségét.
válasz A
144 pm
válasz b
10,5 g/cm3
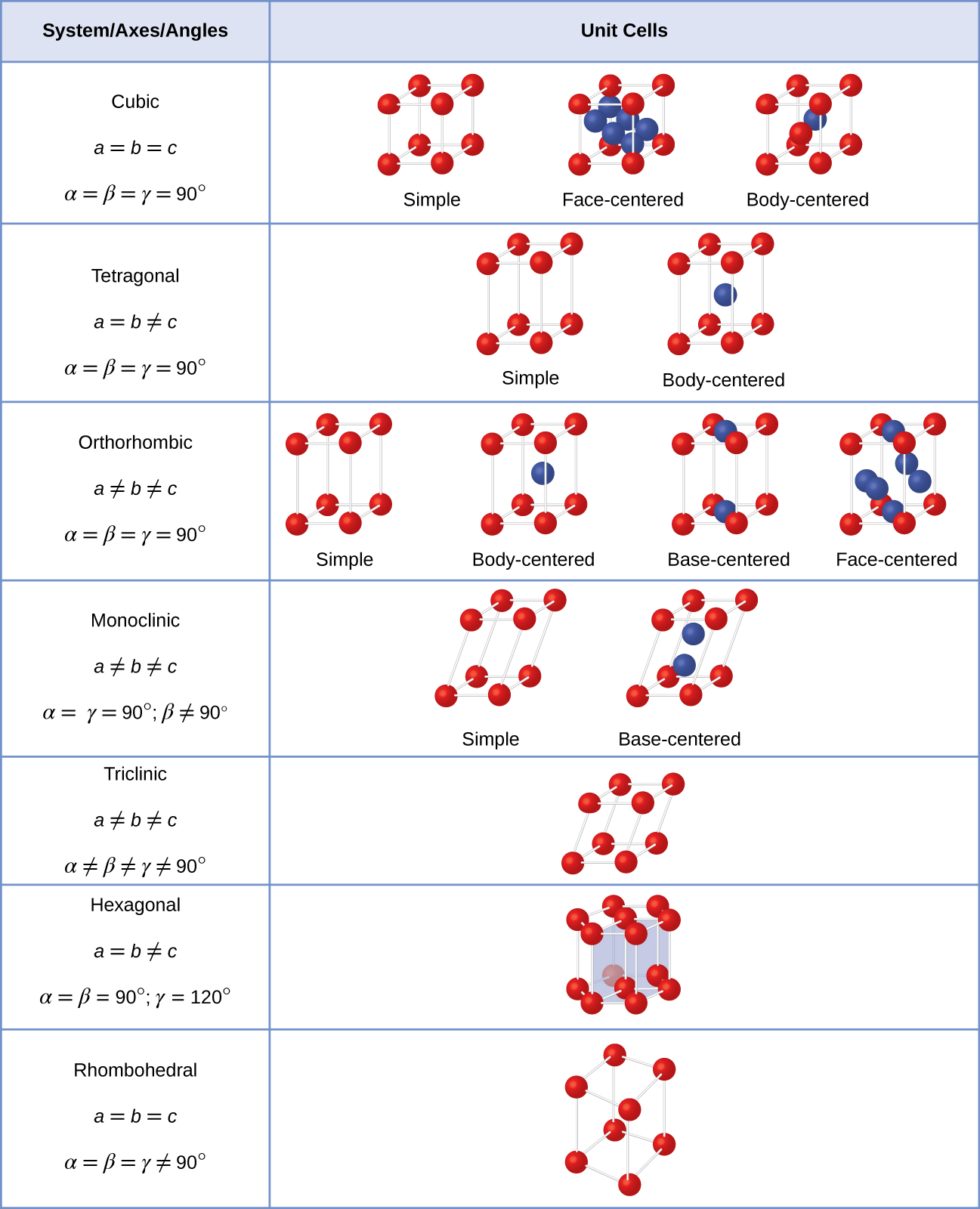
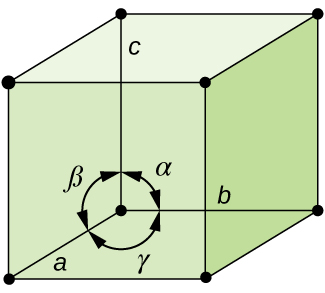
általában egy egységcellát három tengely (a, b, és c) hossza és a közöttük lévő szögek (α, β és γ) határoznak meg, amint azt a \(\PageIndex{10}\) ábra szemlélteti., A tengelyeket úgy definiálják, mint a térrács pontjai közötti hosszúságot. Következésképpen az egységcellás tengelyek azonos környezetekkel csatlakoznak a pontokhoz.
hét különböző rácsrendszer létezik, amelyek közül néhány egynél több típusú rácsot tartalmaz, összesen tizennégy különböző egységcellára, amelyek alakja a \ábrán látható (\PageIndex{11}\).