6.3: Absolute Configuration and the (R) and (s) System (Magyar)
Absolute Configurations of Perspective Formuls
Chemists need a convenious way to different one stereoisomer from another. A Cahn-Ingold-Prelog rendszer olyan szabályrendszer, amely lehetővé teszi számunkra, hogy egyértelműen meghatározzuk bármely sztereokémiai konfigurációt, az “R” (a Latin rectusból, azaz jobbkezes) vagy ” S ” (a Latin Balkezes, azaz Balkezes) jelölésekkel.,
a sztereokémiai nómenklatúra rendszerének szabályai A felszínen meglehetősen egyszerűek.
az R/S kijelölés királis központhoz való hozzárendelésének szabályai
1: rendeljen prioritásokat a négy szubsztituenshez, az #1 pedig a legmagasabb prioritás, a #4 pedig a legalacsonyabb. A prioritások az atomszámon alapulnak.
2: Trace a circle from # 1 to # 2 to # 3.
3: határozza meg a #4 prioritási csoport tájolását. Ha az oldal síkjába van irányítva (tőled távol), lépjen a 4a. lépésre.Ha az oldal síkjából (felé) irányul, lépjen a 4b. lépésre.,
4A: (#4 csoport, amely távol van tőled): a 2.részben az óramutató járásával megegyező kör felel meg az R konfigurációnak, míg az óramutató járásával ellentétes kör megfelel az S konfigurációnak.
4B: (#4 csoport maga felé mutat): a 2. részben az óramutató járásával megegyező kör felel meg az S konfigurációnak, míg az óramutató járásával ellentétes kör megfelel az R konfigurációnak.
első példánkként a 3 szén-dioxid-cukor gliceraldehidet használjuk. Az első dolog, amit meg kell tennünk, hogy prioritást rendeljünk a királis központhoz kötött négy szubsztituens mindegyikéhez., Először megnézzük azokat az atomokat, amelyek közvetlenül kapcsolódnak a királis központhoz: ezek H, O (a hidroxilban), C (az aldehidben), C (A CH2OH csoportban).
R/S konfiguráció hozzárendelése a gliceraldehidhez:

két prioritás egyszerű: a hidrogén, amelynek atomszáma 1, a legalacsonyabb (#4) prioritás, a hidroxil-oxigén pedig a 8-as atomszámmal az 1.prioritás. A szén atomszáma 6. A két ” C ” csoport közül melyik a 2. prioritás, az aldehid vagy a CH2OH?, Ennek meghatározásához még egy kötést távolítunk el a királis központtól: az aldehid esetében kettős kötésünk van az oxigénhez, míg a CH2OH csoportban egyetlen kötés van az oxigénhez. Ha az atom azonos, akkor a kettős kötések elsőbbséget élveznek, mint az egyszeri kötések. Ezért az aldehidcsoportot #2 prioritással, a CH2OH csoportot pedig #3 prioritással látják el.
prioritásainkkal a 4. prioritási csoportot (a hidrogént) tekintjük, és látjuk, hogy távol van tőlünk, az oldal síkjába mutatunk-így a fenti eljárás 4A lépése érvényes., Ezután nyomon követünk egy kört, amelyet az #1, #2 és #3 prioritási csoportok határoznak meg, növekvő sorrendben. A kör az óramutató járásával megegyező irányban van, ami a 4a. lépésben azt mondja, hogy ennek a szénnek ” R ” konfigurációja van, és hogy ez a molekula (R)-gliceraldehid. Enantiomerjének definíció szerint (s)-gliceraldehidnek kell lennie.
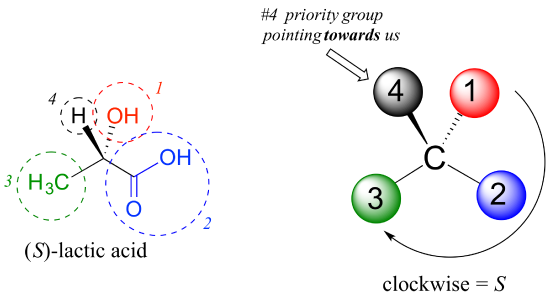
ezután nézzük meg a tejsav egyik enantiomerjét, és határozzuk meg a királis központ konfigurációját. Nyilvánvaló, hogy H A #4 szubsztituens, OH pedig # 1. Az oxigénnel való három kötése miatt a savcsoporton lévő szén elsőbbséget élvez #2, a metil-csoport pedig #3., A # 4 csoportot, a hidrogént, véletlenül felénk (az oldal síkjából) húzzuk ebben az ábrán, tehát a 4B lépést használjuk: az 1-től #2-ig #3-ig terjedő kör az óramutató járásával megegyező irányban van, ami azt jelenti, hogy a királis Központ s konfigurációval rendelkezik.
a gyógyszer talidomid egy érdekes, de tragikus esettanulmány a sztereokémia fontosságáról a gyógyszertervezésben., Először gyártott egy német gyógyszeripari vállalat által előírt széles körben Európában és Ausztráliában az 1950-es évek végén, mint egy nyugtató és orvosolja a reggeli rosszullét terhes nők, talidomid hamarosan érintett, mint az oka a pusztító születési rendellenességek csecsemőknél született nők, akik vették. A talidomid királis központot tartalmaz, így két enantiomer formában létezik. Racém keverékként forgalmazták: más szóval, mindkét enantiomer 50: 50 keveréke.
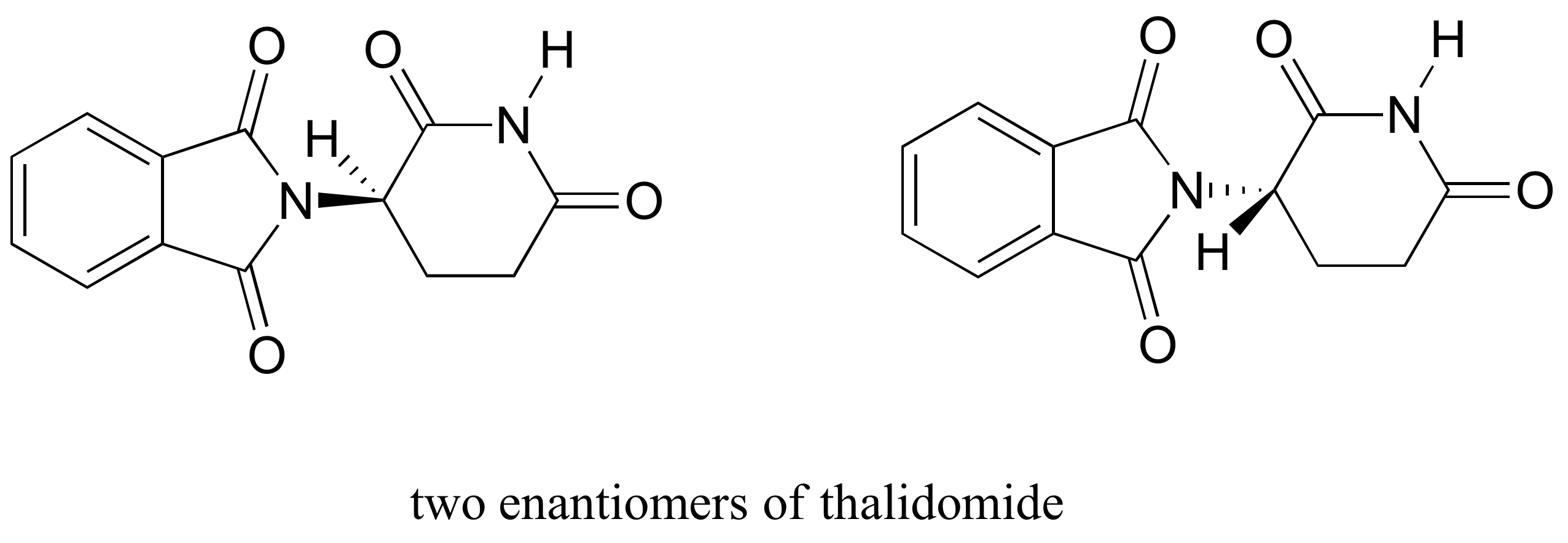
próbáljuk meg meghatározni az enantiomer sztereokémiai konfigurációját a bal oldalon., A királis központhoz vezető négy kötés közül a #4 prioritás a hidrogén. A nitrogéncsoport #1, A Gyűrű karbonil oldala # 2, A Gyűrű-CH2 oldala #3.
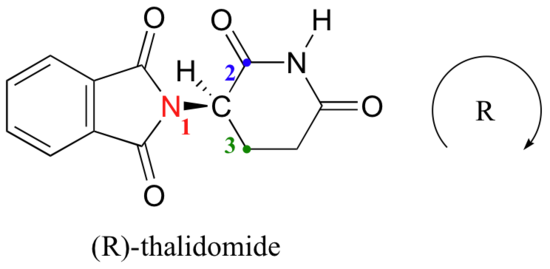
a hidrogén elénk mutat, és a priorizált szubsztituensek egy óramutató járásával megegyező kört követnek: ez a talidomid R enantiomere. A másik enantiomernek természetesen rendelkeznie kell az S konfigurációval.,
bár a tudósok ma még nem tudják, hogyan működik a talidomid, a kísérleti bizonyítékok arra utalnak, hogy valójában az R enantiomer volt a kívánt orvosi hatás, míg az S enantiomer okozta a születési rendellenességeket. Még ezzel a tudással sem a tiszta (R) – talidomid nem biztonságos, mert a szervezetben lévő enzimek gyorsan átalakulnak a két enantiomer között-látni fogjuk, hogy ez hogyan történik a 12.fejezetben.
történelmi megjegyzésként a talidomidot soha nem hagyták jóvá az Egyesült Államokban történő alkalmazásra. Ez nagyrészt Dr., Frances Kelsey, egy élelmiszer-és kábítószer-tiszt, aki, veszélyben a karrierje, blokkolta a jóváhagyás miatt neki aggodalmak hiánya megfelelő biztonsági vizsgálatok, különös tekintettel a gyógyszer képes belépni a véráramba a fejlődő magzat. Sajnos azonban abban az időben az új gyógyszerek klinikai vizsgálatai széles körben elterjedtek és szabályozatlanok voltak az orvosok és betegeik számára szerte az országban, így az amerikai családokat nem kímélték az okozott károktól.,
nemrégiben a talidomid közeli származéka jogszerűvé vált az Egyesült Államokban, szigorú biztonsági intézkedések betartásával, a myeloma multiplexnek nevezett vérrák kezelésére. Brazíliában a talidomidot a lepra kezelésére használják – de a biztonsági intézkedések ellenére a gyermekek még mindig talidomiddal kapcsolatos hibákkal születnek.
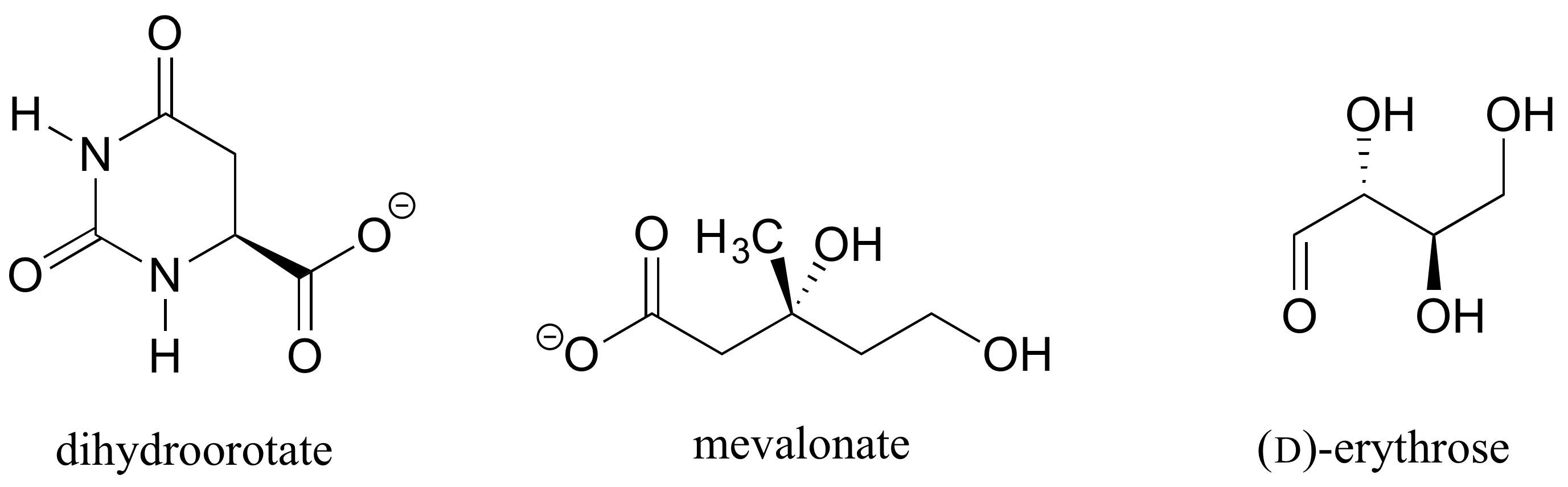
1. gyakorlat.: Határozza meg a királis központok sztereokémiai konfigurációit az alábbiakban bemutatott biomolekulákban.
2.gyakorlat.,: A malát (R) enantiomerének szilárd vagy szaggatott ékkel kell rendelkeznie az alábbi ábrán látható C-O kötéshez?
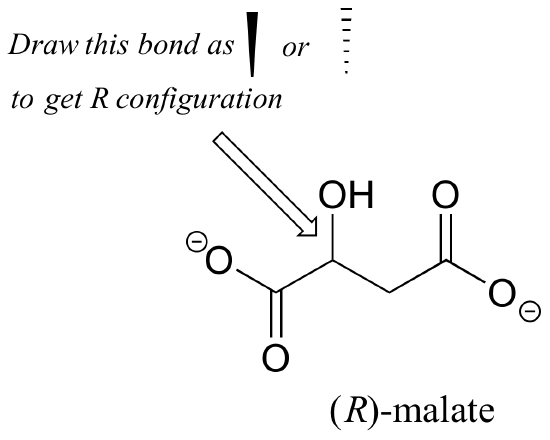
3.gyakorlat.: Szilárd vagy szaggatott ékek segítségével sztereokémiát mutatva húzzuk meg az ibuprofen (R) enantiomerjét és a 2-metileritrit-4-foszfát (a struktúrákat ebben a fejezetben korábban sztereokémia nélkül mutatjuk be).
megoldások gyakorlatok
abszolút konfigurációk Fischer előrejelzések
meghatározásához az abszolút konfiguráció egy királis központ egy Fisher vetület, használja a következő kétlépcsős eljárás.,
1. Lépés
prioritási számokat rendeljen a királis központhoz kötött négy ligandumhoz (csoporthoz) a CIP prioritási rendszer segítségével.
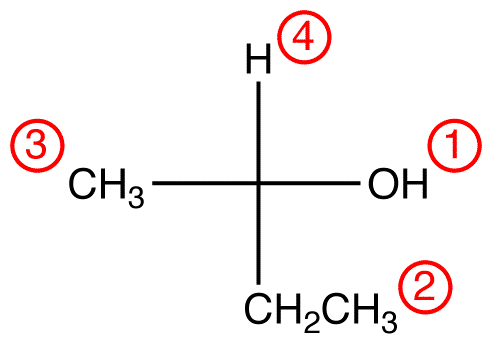
2.lépés – függőleges opció
Ha a legalacsonyabb prioritású ligand függőleges kötésen van, akkor a nézőtől távol helyezkedik el.
Kövesse nyomon a három legmagasabb prioritású ligandumot a legmagasabb prioritású ligandumtól ( ① → ② → ③ ) kezdve abba az irányba, amely nagyon helyes választ ad.

az alábbi vegyületben a mozgás az óramutató járásával megegyező irányban jelzi az R-konfigurációt., Ennek a vegyületnek a teljes IUPAC neve (R)-bután-2-ol.

2.lépés – vízszintes opció
Ha a legalacsonyabb prioritású ligandum vízszintes kötésen van, akkor a néző felé mutat.
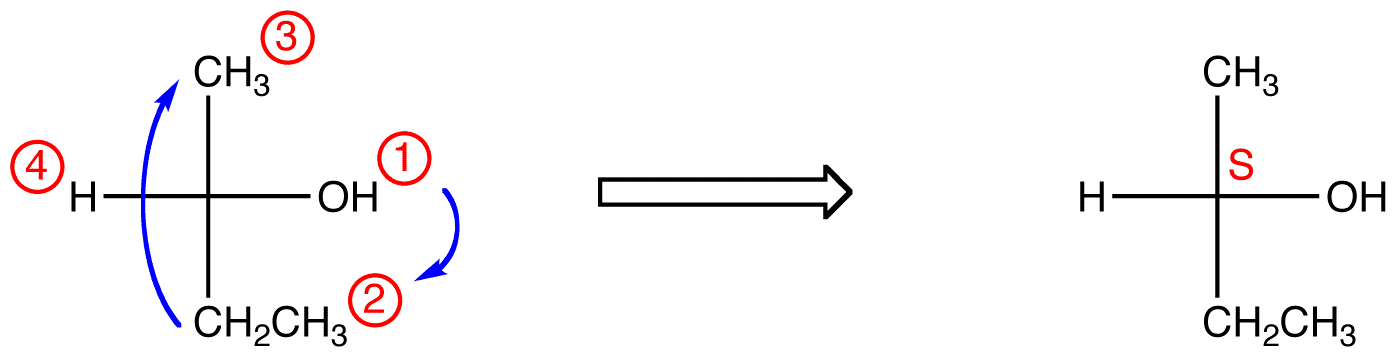
Kövesse nyomon a három legmagasabb prioritású ligandumot a legmagasabb prioritású ligandumtól ( ① → ② → ③ ) kezdve abba az irányba, amely szörnyen rossz választ ad. Vegye figyelembe az alábbi táblázatban, hogy a konfigurációk megfordul az első példától.,
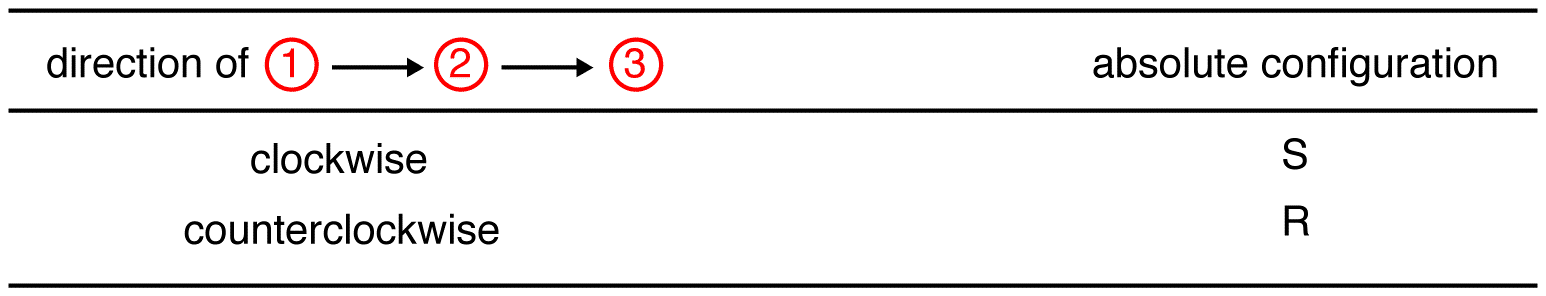
az alábbi vegyületben a mozgás az óramutató járásával megegyező (R), ami rettenetesen rossz, tehát a tényleges konfiguráció S. ennek a vegyületnek a teljes IUPAC neve (s)-butan-2-ol.
A Fischer-vetületek módosítása nélkül
a Fischer-vetület két dimenzióra korlátozza a háromdimenziós molekulát. Következésképpen vannak korlátozások a Fischer-vetítésen elvégezhető műveletekre anélkül, hogy megváltoztatnák a királis központokban az abszolút konfigurációt., Azok a műveletek, amelyek nem változtatják meg az abszolút konfigurációt egy királis központban egy Fischer-előrejelzésben, két szabályként foglalhatók össze.
1. szabály: a Fischer-vetület 180º-os elforgatása mindkét irányban anélkül, hogy felemelné a papír síkjáról, nem változtatja meg a királis központ abszolút konfigurációját.
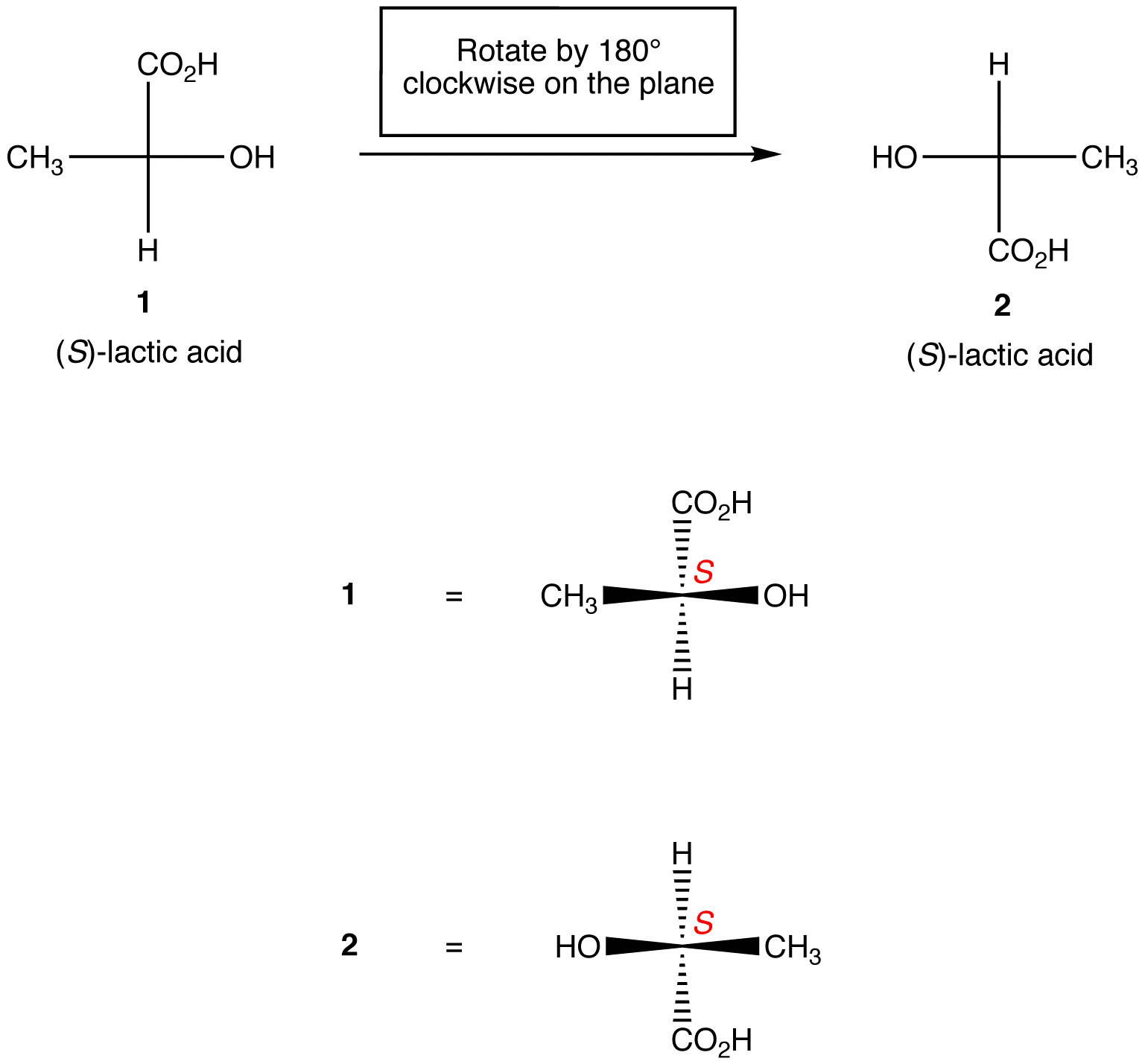
2.szabály: három ligandum elforgatása a királis középponton mindkét irányban, a fennmaradó ligandumot a helyén tartva, nem változtatja meg az abszolút konfigurációt a királis központban.,
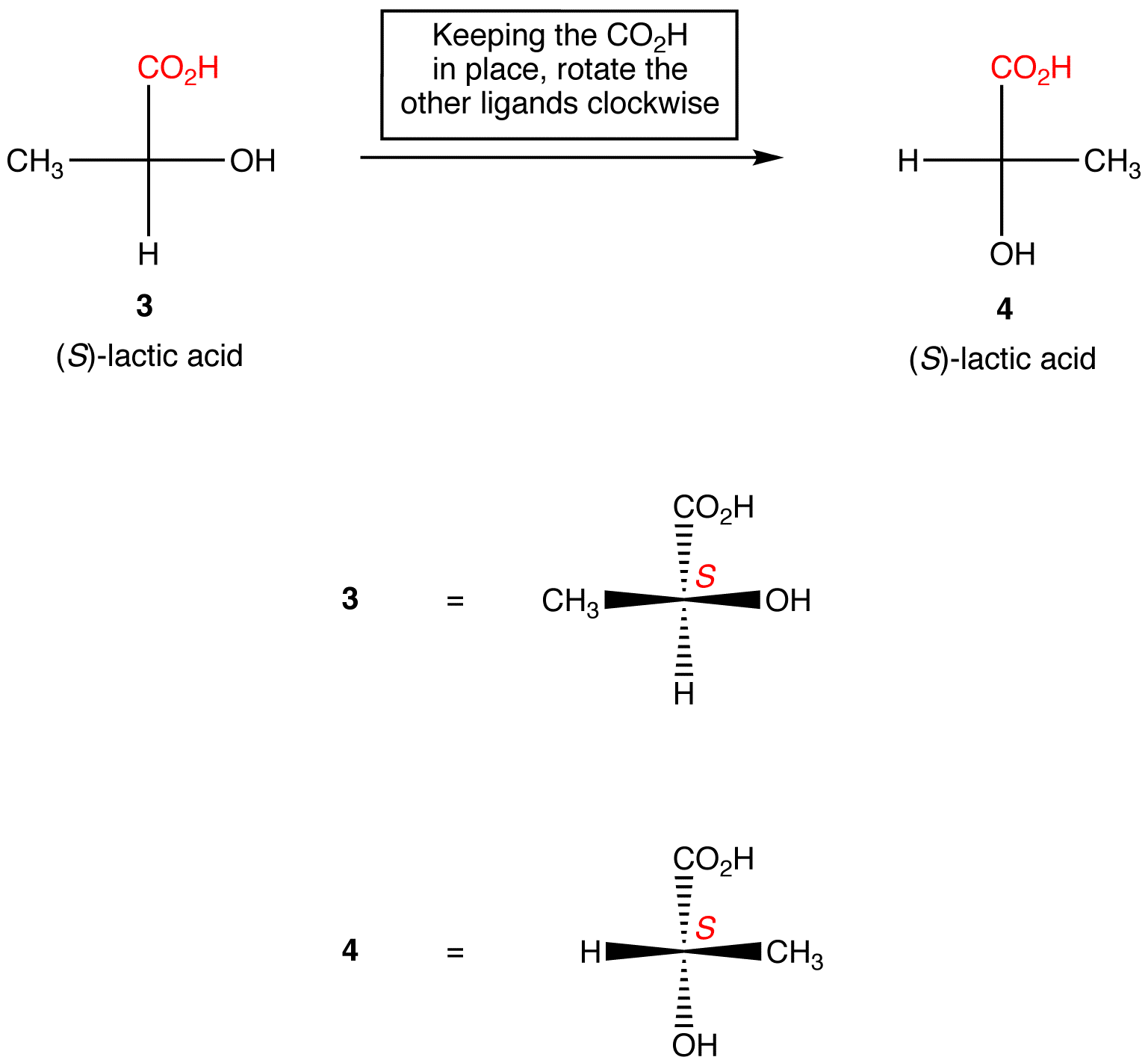
manipulálása Fischer előrejelzések módosítása konfiguráció
a műveleteket, amelyek megváltoztatják az abszolút konfiguráció egy királis központ egy Fischer vetítés lehet összefoglalni, mint két szabály.
1. szabály: a Fischer-vetület 90º-os elforgatása mindkét irányban megváltoztatja az abszolút konfigurációt a királis központban.
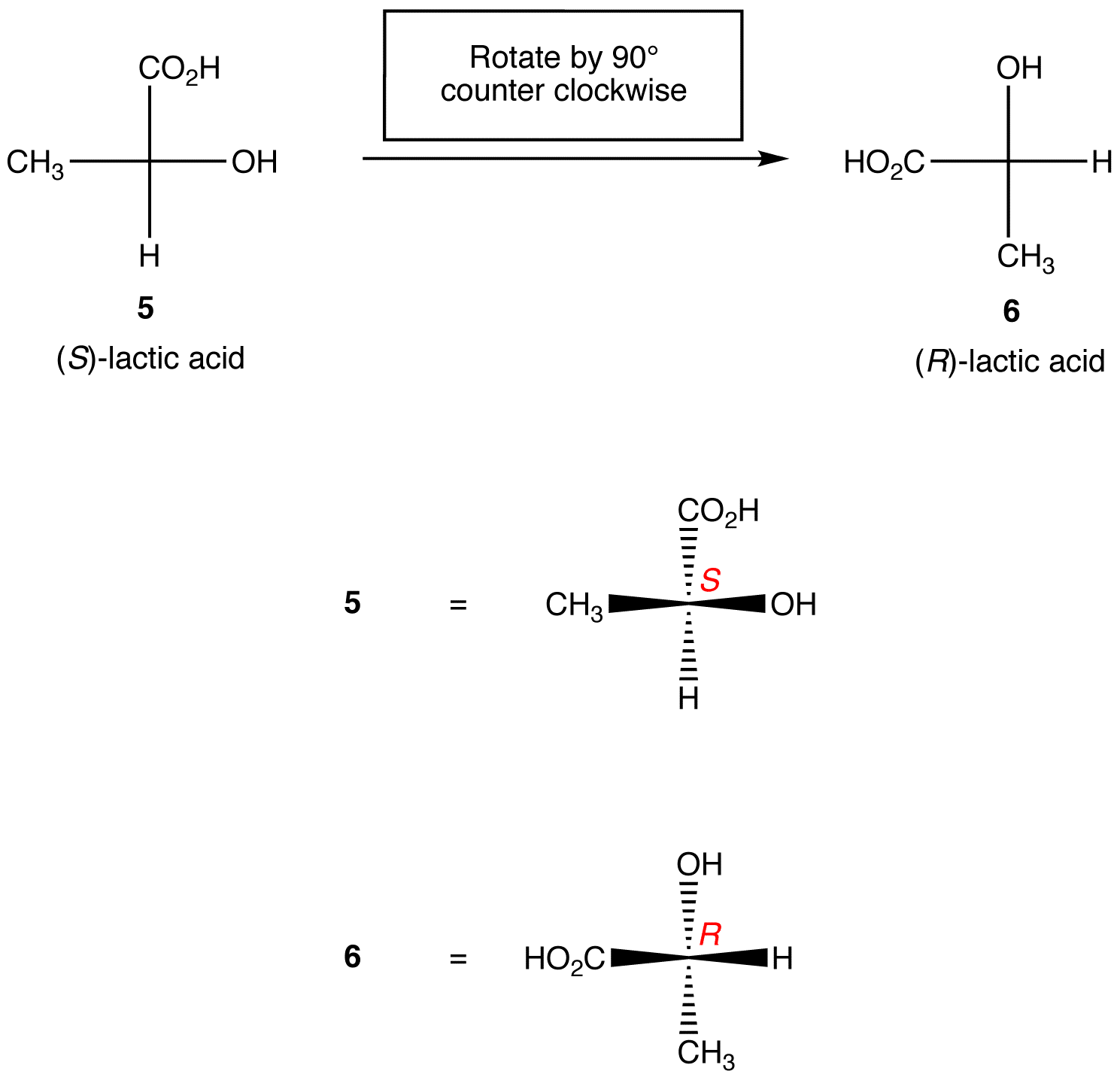
2. szabály: bármely két ligandum felcserélése a királis központban megváltoztatja az abszolút konfigurációt a királis központban.,
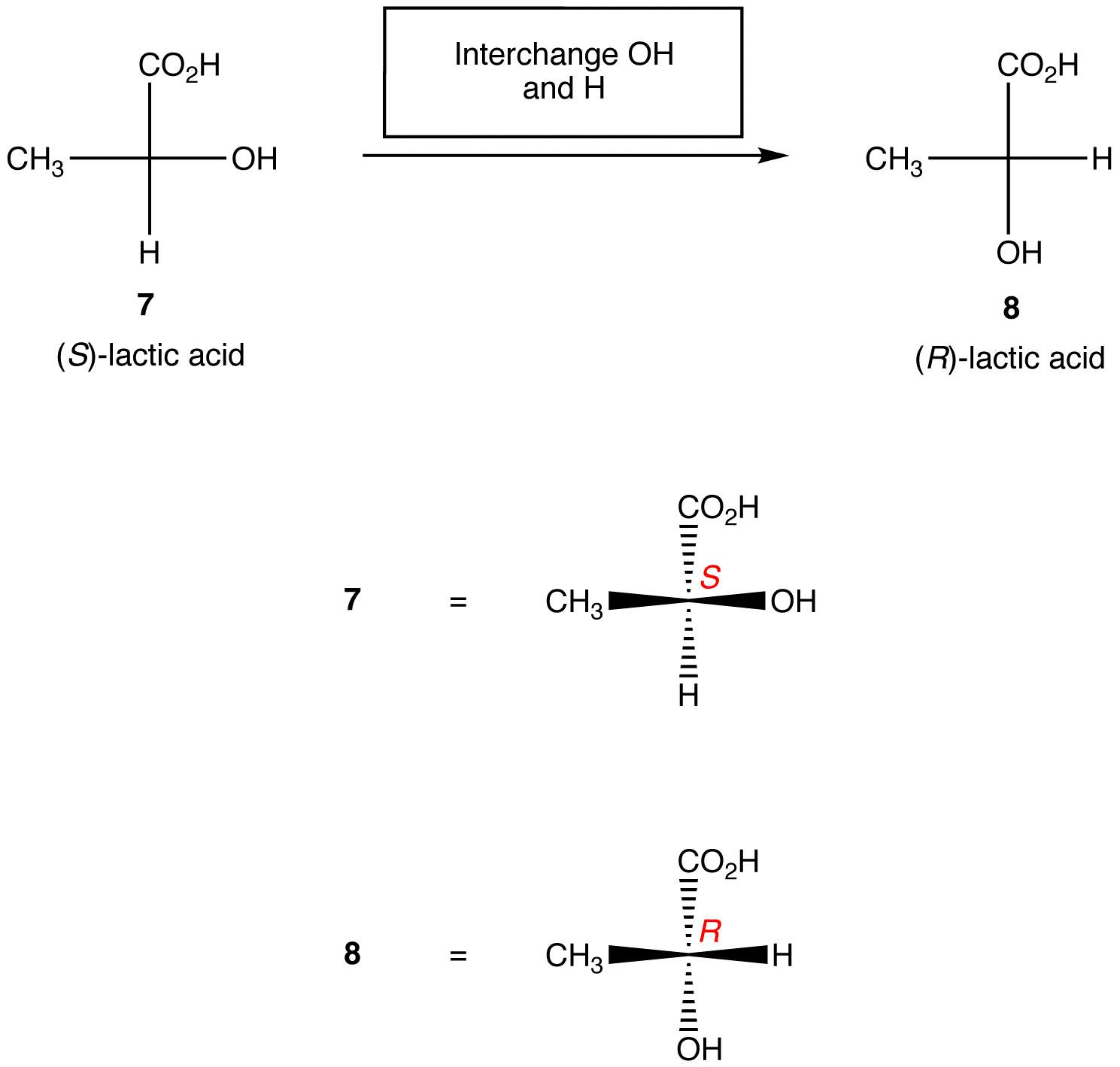
a fenti szabályok azt feltételezik, hogy a vizsgált Fischer-vetület csak egy királis központot tartalmaz. Azonban óvatosan alkalmazhatók a Fischer vetületekre, amelyek tetszőleges számú királis Központot tartalmaznak.
1. gyakorlat
osztályozza a következő vegyületeket R vagy S?
- S: I >Br>F>F> H. a legalacsonyabb prioritású szubsztituens, h, már hátul megy., Balra fordul, I-ről Br-re F – re, tehát S.
- r: Br > Cl > CH3 > H. a H-t és a Br-t át kell váltani, hogy a H-t, a legalacsonyabb prioritást, hátul helyezze el. Ezután br-ről Cl-re haladva a CH3 jobbra fordul, így R.
- sem R, sem S: Ez a molekula achirális. Csak királis molekulák nevezhetők R vagy S.
- R: OH > CN > CH2NH2 > H. a H, a legalacsonyabb prioritás, vissza kell kapcsolni., Ezután az OH-tól a CN-ig CH2NH2-ig jobbra fordul, így R.
- (5) S: \(\ce {- COOH}\) > \(\ce {- CH_2OH}\) > \(\ce{c#CH}\) > \(\CE{H}\). Ezután a \(\ce{-COOH}\)-tól \(\ce {- CH_2OH}\) – ig \(\ce {- C#CH}\) balra fordul, S konfigurációt adva.
gyakorlatok
6. Irányítsa a következőket úgy, hogy a legkisebb prioritás (4) atom mögött legyen, majd rendeljen sztereokémiát (R vagy S).

7. Döntetlen (R)-2-brómbután-2-ol.
8., R/S hozzárendelése a következő molekulához.
.png?revision=1)

A = S; B = r
8. A sztereó központ R.
egyéb források
Kahn Academy video tutorial on the R-S Name system
- Schore and Vollhardt. Szerves kémiai szerkezet és funkció. New York: W. H. Freeman and Company, 2007.
- McMurry, John and Simanek, Eric. A szerves kémia alapjai. 6. Szerk. – Brooks Cole, 2006.,
közreműködők és hozzárendelések
- Ekta Patel (UCD), Ifemayowa Aworanti (Maryland Baltimore Megyei Egyetem)
- Szerves Kémia, biológiai hangsúlyozással Tim Soderberg (Minnesota Egyetem, Morris)