Electron cloud facts for kids (Italiano)

Le forme dei primi cinque orbitali atomici sono: 1s, 2s, 2px, 2py e 2pz. I due colori mostrano la fase o il segno della funzione d’onda in ogni regione. Questi sono grafici delle funzioni ψ(x, y, z) che dipendono dalle coordinate di un elettrone. Per vedere la forma allungata delle funzioni ψ(x, y, z)2 che mostrano più direttamente la densità di probabilità, vedere i grafici degli orbitali d di seguito.
Nube di elettroni è un termine informale in fisica., È usato per descrivere dove sono gli elettroni quando girano intorno al nucleo di un atomo.
Il modello di nube di elettroni è diverso dal vecchio modello atomico di Bohr di Niels Bohr. Bohr ha parlato di elettroni che orbitano attorno al nucleo. Spiegare il comportamento di queste “orbite” di elettroni era una questione chiave nello sviluppo della meccanica quantistica.
Il modello di nube di elettroni dice che non possiamo sapere esattamente dove un elettrone è in un dato momento, ma gli elettroni sono più probabilità di essere in aree specifiche., È teoricamente possibile, per un elettrone di essere una distanza quasi infinita dal nucleo atomico è in orbita, anche se la probabilità di un elettrone diminuisce drasticamente il più lontano dal nucleo si cerca. Questo è il modo più moderno e accettato per descrivere la situazione.
Nel modello di Bohr, gli elettroni sono stati assegnati a gusci diversi. Questi gusci spiegavano i modelli ripetuti delle proprietà chimiche nella tavola periodica. Utilizzando la meccanica quantistica, i chimici possono utilizzare il modello di nube di elettroni per assegnare elettroni a diversi orbitali atomici., Questi orbitali atomici non sono tutte sfere. Gli orbitali atomici spiegano anche i modelli nella tavola periodica.
Il modello di nube di elettroni è stato sviluppato nel 1925 da Erwin Schrödinger e Werner Heisenberg. Il modello è un modo per aiutare a visualizzare la posizione più probabile di elettroni in un atomo. Il modello di nube di elettroni è l’attuale modello accettato di un atomo.,d=”345ec9c6a1″>
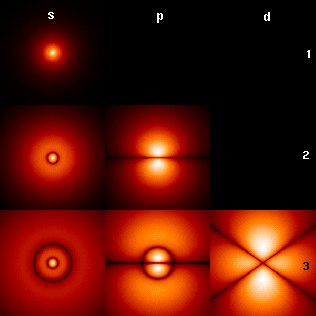
Falso-colore densità immagini di alcuni idrogeno come orbitali atomici (f orbitali e superiore non vengono visualizzati)

Sperimentalmente ripresi 1s e 2p core-elettroni orbitali di Sr, compresi gli effetti dell’atomica vibrazioni termiche e di eccitazione in ampliamento, recuperati da energy dispersive x-ray spectroscopy (EDX) in scansione microscopia elettronica a trasmissione (STAMINALI).,