Combinado de terapia neonatal hipóxico-isquémica encefalopatia | Anales de Pediatría (Edição em inglês)
Introdução
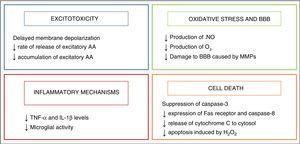
Com uma incidência de 1-3 casos por 1000 nascidos a termo nascimentos,1 hipóxico-isquémica encefalopatia (HIE) é uma das causas mais frequentes de lesões cerebrais em recém-nascidos. Tendo em conta o número crescente de nascimentos de alto risco devido às tendências crescentes da idade materna e da frequência de gravidezes múltiplas, entre outros fatores, o HIE continua a ser um problema relevante no ambiente hospitalar para o qual ainda não existe uma solução definitiva.,a investigação sobre a fisiopatologia da asfixia perinatal permitiu-nos compreender o processo complexo que ocorre nos níveis celular e tecidular à medida que a lesão cerebral se desenvolve devido à falta de oxigénio. Muitos dos mecanismos de lesão envolvidos são agrupados com base no tempo decorrido para o seu desenvolvimento, e quatro fases principais foram descritas (Fig. 1): fase primária ou episódio agudo de isquémia hipóxica (HI), fase latente, fase secundária e fase terciária., Na fase primária, os danos resultam de uma redução no fornecimento de oxigênio para células e tecidos, o que resulta em falha de energia primária. Isto é seguido por uma recuperação aparente nos níveis de compostos fosforilados de alta energia, conhecidos como a fase latente., No entanto, esta melhoria é apenas temporário e dá lugar para a segunda fase, quando muitos dos mecanismos fisiopatológicos envolvidos no desenvolvimento de lesões cerebrais em recém-nascidos entram em jogo, o chefe de que são excitotoxicity, um enorme influxo de íons cálcio para dentro das células, estresse oxidativo, inflamação e, na maioria dos casos, a morte celular por apoptose ou necrose. Por último, a fase terciária caracteriza-se pela persistência de lesões cerebrais semanas, meses ou mesmo anos após o insulto hipóxico-isquémico inicial.,
a compreensão da fisiopatologia subjacente do HIE permitiu a identificação de potenciais alvos terapêuticos que poderiam ajudar a reduzir os danos cerebrais causados pela asfixia e o desenvolvimento de numerosas estratégias de tratamento. Alguns destes tratamentos, atualmente em ensaios, destinam-se a trabalhar sinergicamente com hipotermia terapêutica, o único tratamento contra HIE que tem sido geralmente adotado no ambiente de cuidados intensivos neonatais.,hipotermia a hipotermia começou a ser utilizada como estratégia neuroprotectora em lactentes após a descoberta de um mecanismo de arrefecimento endógeno que se manifestou em lactentes que sofreram algum tipo de lesão durante o nascimento.Os seus efeitos neuroprotectores estão principalmente relacionados com a diminuição da actividade metabólica do cérebro, de 5% a cada diminuição de 1°C na temperatura,3 que modula algumas das vias metabólicas prejudiciais desencadeadas pela asfixia, que são resumidas na Fig. 2.
terapia de Combinação
uma vez que as provas sugerem que os atuais hipotermia protocolos são optimal4, no entanto, são de eficácia limitada na prática clínica,5 precisamos expandir estão arsenal terapêutico para a gestão da HIE.,6 pesquisas Recentes têm focado no desenvolvimento e implementação de tratamentos que podem ser usados em combinação com hipotermia, projetado para atuar em diferentes níveis de fisiopatológicos cascata e promover a sinergia de ambas as terapias (Fig. 3).

Melatonina
a Melatonina (N-acetil-5-metoxitriptamina) é um neurohormone sintetizado pela glândula pineal, cuja secreção segue uma noite/dia do ciclo e cuja principal função é na regulação do ritmo circadiano. Os aspectos-chave que permitem o seu uso na gestão do HIE são a sua poderosa actividade7 antioxidante e anti-inflamatório e a sua capacidade de atravessar a barreira hemato-encefálica e chegar ao sistema nervoso central.,8
Antes de ser julgado em recém-nascidos, a melatonina demonstrou aumentar o nível de protecção proporcionado pela hipotermia através da optimização do metabolismo da energia cerebral num modelo de piglet de asfixia.9 no contexto clínico, um estudo publicado por Aly et al.10 atribuíram metade dos recém-nascidos asfixiados à hipotermia e 5 doses de 10 mg/kg/dia de melatonina administradas por via oral., Os autores encontraram uma redução nos níveis séricos de superóxido dismutase e óxido nítrico nos doentes tratados com terapêutica combinada em comparação com os tratados apenas com arrefecimento, demonstrando assim os efeitos benéficos da combinação de ambas as estratégias contra o stress oxidativo.um estudo recente conduzido por Balduini et al., para avaliar a segurança, farmacocinética, dosagem e eficácia da melatonina utilizada em associação com hipotermia, verificou-se que o arrefecimento não afectou a farmacocinética da melatonina11 e que foi possível obter níveis séricos elevados da hormona que administra doses inferiores às utilizadas em modelos experimentais animais. Actualmente, o ensaio clínico MELPRO (NCT03806816) está a recrutar doentes, visando uma amostra de 100 recém-nascidos., Este e outros estudos semelhantes são indispensáveis para o desenvolvimento futuro de ensaios clínicos de fase III e para o uso subsequente de melatonina na prática clínica diária.
alopurinol
a razão para a utilização de alopurinol no tratamento do HIE é o seu efeito inibitório na xantina oxidase, uma enzima envolvida no stress oxidativo. Além disso, esta droga actua como um quelante de ferro livre e sequestra radicais hidroxilo.,12,13 um estudo pré-clínico em crias de rato, em que os animais foram distribuídos a 1 de 5 grupos (Grupo de controlo, grupo IH, grupo tratado com hipotermia, grupo tratado com alopurinol e grupo tratado com terapêutica combinada) concluiu que 72h após o HI insulto, o grupo de terapêutica combinada exibia o menor volume de enfarte.,14
Quando se trata de suas características farmacológicas, alopurinol pode rapidamente atravessar a placenta e atingir concentrações terapêuticas em recém-nascidos, como demonstrado em um estudo realizado em mulheres grávidas que receberam 500 mg de alopurinol por via intravenosa, com evidências de níveis ideais de alopurinol 5min mais tarde, em amostras de sangue de cordão umbilical.15 um estudo realizado por van Bel et al., em 1998, que analisou o seu potencial efeito antioxidante em recém-nascidos asfixiados com HIE grave, concluiu que a administração intravenosa de 40 mg/kg de alopurinol atingiu uma redução na formação de radicais livres.13 No entanto, um estudo realizado mais tarde por Benders et al. em 2006, não foram encontradas diferenças entre o grupo tratado com alopurinol e o grupo controlo.16 nas conclusões, estes autores identificaram a extrema gravidade do HIE nos recém-nascidos incluídos na amostra como uma possível explicação para a falta de diferenças significativas., Além disso, a Comissão formulou a hipótese de que o período decorrido até à administração do alopurinol (3–4h após a reperfusão) poderia ter sido demasiado longo para alcançar resultados favoráveis. Em relação ao último ponto, Gunes et al. administrou a mesma dose de alopurinol administrada nos 2 estudos anteriores, mas dentro de 2h desde o nascimento, e encontrou melhorias nos resultados do desenvolvimento neurológico no grupo de tratamento.,De acordo com as mesmas linhas, a administração de alopurinol intravenoso a mães durante o parto de fetos com hipoxia ou hipoxia incipiente aumentou a eficácia do tratamento, reduzindo os níveis sanguíneos do cordão umbilical da proteína S-100β, que é um marcador de danos cerebrais.Um ensaio clínico com o nome de efeito do alopurinol na lesão cerebral hipóxica-isquémica no resultado neurocognitivo (NCT03162653) está actualmente em curso para avaliar os potenciais efeitos terapêuticos da administração deste inibidor enzimático nos primeiros minutos após o nascimento.,a eritropoietina(EPO) é uma citoquina com 30, 4 kDa sintetizada pelo fígado na vida fetal e após o nascimento pelo rim e pelo cérebro em desenvolvimento, onde actua como factor de crescimento e agente neuroprotector.19 O uso tanto de EPO e EPO humana recombinante (rhEPO) na HIE, com base na sua atividade, por meio do envolvimento de EPO receptores presentes em neurônios e glia,20 como um potente agente anti-apoptótica (estimulando a transcrição de genes anti-apoptótica BCL-2 e BCL-XL), e como um anti-inflamatório e antioxidante.,19,21 além de seu efeito neuroprotetor, EPO pode promover processos de reparo a longo prazo, tais como angiogênese, oligodendrogênese e neurogênese.Os estudos pré-clínicos que avaliaram o efeito sinérgico da combinação da administração de EPO ou rhEPO com hipotermia produziram resultados contraditórios. Num modelo semelhante no rato de lesão cerebral hipóxica-isquémica no dia 7 após o nascimento, Fang et al. não encontrei efeitos neuroprotectores significativos do seu uso combinado.No entanto, num outro estudo realizado por Fan et al.,, 25 os autores observaram um efeito benéfico ligeiro na função sensorimotora das crias de rato, embora esta diferença não se tenha reflectido nas características histológicas das amostras de tecido cerebral.estudos em recém-nascidos com HIE demonstraram que a utilização de rhEPO é segura com doses de 300–2500 UI/kg. Doses baixas de rhEPO foram consideradas eficazes em doentes com danos moderados, e parecem estar associadas a uma diminuição do risco de incapacidade ou morte.Doses mais elevadas (até 2500 UI / kg) podem reduzir a incidência de convulsões e anomalias neurológicas aos 6 meses.,27
Hoje, três de fase III de ensaios clínicos estão em andamento com um planejada de recrutamento de um total de 840 recém-nascidos para avaliar a segurança e a eficácia de altas doses de EPO (1000IU/kg), combinado com hipotermia (Eritropoietina para Hipóxico Isquêmica do Encefalopatia em recém-nascidos, NCT03079167; Alta dose de Eritropoietina por Asfixia e Encefalopatia, NCT02811263; a Eritropoietina na Gestão dos Neonatal Hipóxico Isquêmica Encefalopatia, NCT03163589). O principal objetivo do primeiro 2 é reduzir a mortalidade ou deficiência de 2 anos, enquanto o terceiro avaliará estes dois resultados após 1 ano., Aguardamos os resultados destes e de outros estudos para determinar se o EPO ou algum dos seus derivados são eficazes e como devem ser utilizados na prática clínica, avaliando factores como a dose mínima eficaz, a via de administração, a duração do tratamento, etc.
células estaminais
O uso de células estaminais para o tratamento de todos os tipos de doenças, incluindo HIE, é um campo de pesquisa que continua a crescer., Esta abordagem terapêutica pode ajudar a reparar e regenerar o tecido cerebral danificado após o insulto hipóxico-isquémico através da interacção das células estaminais com as células imunitárias em órgãos distantes do cérebro, tais como o baço, alterando assim a resposta imunológica/inflamatória. Do mesmo modo, a recuperação funcional alcançada com a sua administração pode ser parcialmente explicada pela interacção das células transplantadas e do tecido cerebral, com a subsequente produção de factores de crescimento cujo efeito final se reflectiria no aumento da neurogénese e da proliferação celular.,
Embora ainda precisamos aprofundar nosso conhecimento para ser capaz de usar células-tronco como uma terapia eficaz, estudos experimentais em animais têm demonstrado que diferentes tipos de células-tronco são capazes de sobreviver no cérebro danificado, se diferenciar em neurônios ou glia, integrar-se com o tecido do alvo e modificar favoravelmente resultados comportamentais (revista em Bennet et al.28)., Estudos recentes têm relatado que a administração de células estaminais mesenquimais combinadas com 24h de arrefecimento em crias de rato 7 dias após o nascimento alcançou melhores resultados em comparação com qualquer um dos tratamentos isolados 29 e também descobriram que a hipotermia expande o período terapêutico para a administração de células estaminais mesenquimais até 2 dias após o acontecimento hipóxico-isquémico.,30 além disso, as células-tronco podem regular a resposta imune através de sua interação com células imunes efetoras localizado em órgãos distantes do cérebro, tais como o baço, cuja mobilização é conhecido por ter o potencial para exacerbar a resposta inflamatória e o dano isquêmico no cérebro imaturo, reforçando assim o seu efeito neuroprotetor.,31,32
a terapia com células Estaminais, sozinho ou em combinação com hipotermia terapêutica, é um campo promissor de pesquisa que ainda requer estudos clínicos para determinar, entre outros aspectos, o mais eficaz tipo de células-tronco e a melhor dosagem e duração do tratamento para obter os melhores resultados do tratamento.,28 Um dos projetos em andamento na fase de recrutamento (Estudo do hCT-MESTRADO em Recém-nascidos Com Moderada ou Grave HIE, NCT03635450) inclui 6 de bebês nascidos em uma idade gestacional de 36 ou mais semanas, com moderada a severa HIE ser tratados com hipotermia e 2 intravenosa, doses de mesenquimais, células do estroma derivadas do cordão umbilical, tecido (hCT-MSC). Os principais objectivos deste ensaio de fase I São avaliar a segurança da hCT-MSC e analisar os resultados da sobrevivência e do desenvolvimento neurológico nos participantes aos 6 e 16 meses, respectivamente., Outro estudo de fase I (NCT00593242) obtido resultados promissores com o transplante autólogo de sangue do cordão umbilical células, com 74% dos recém-nascidos que receberam células-tronco sobrevivendo com pontuação de 85% ou superior em escalas Bayley comparação com 41% dos recém-nascidos tratados com refrigeração sozinho.33
N-acetilcisteína
N-acetilcisteína (NAC) é um precursor da cisteína que elimina radicais livres e está envolvido na manutenção da glutationa,34 assim regulando o estresse oxidativo., As provas de modelos animais revelaram uma maior redução do volume de enfarte cerebral em animais tratados com uma combinação de ácido acetilsalicílico e hipotermia em comparação com animais tratados com apenas uma destas intervenções. Além disso, os animais tratados com terapêutica combinada apresentaram resultados semelhantes, em reflexos e lesões da matéria branca, aos encontrados no grupo de controlo.Uma vez que a sua administração durante a gravidez não tem efeitos teratogénicos e pode atravessar a placenta,36 CNA passou a ser considerado um dos agentes terapêuticos mais promissores para utilização futura em unidades de cuidados intensivos neonatais., No entanto, tanto quanto sabemos, até à data não foram concebidos ensaios clínicos para avaliar a sua utilização na gestão do HIE, e a evidência disponível limita-se a ensaios relacionados com inflamação intra-amniótica, corioamnionite ou síndrome de dificuldade respiratória.gases nobres como o xénon e o radão exibiram efeitos neuroprotectores em modelos animais de HI neonatal. Numerosos estudos analisaram a possibilidade de utilizar o xénon como agente terapêutico (para uma revisão da evidência, ver o artigo de Lobo et al.,37) devido à sua capacidade de reduzir a excitotoxicidade após um HI insulto através da modulação dos receptores de glutamato NMDA.38, 39
no ensaio clínico multicêntrico, a hipotermia total do corpo e o xénon (TOBY-Xe) utilizaram gás de xénon em combinação com hipotermia numa amostra de 92 lactentes nascidos entre 36 e 43 semanas de gestação., Apesar de não encontrar diferenças significativas entre os grupos,de 40, com o objectivo de obter informação mais detalhada sobre algumas das variáveis que podem ter tido um impacto sobre os resultados do tratamento com este nobre gás, tais como a sua dosagem ou duração, de um ensaio clínico de fase II está em andamento (CoolXenon3 Estudo, NCT02071394).,
Por outro lado, até à data não foram realizados ensaios clínicos com argon, mas demonstrou-se que argon melhora os resultados do arrefecimento em termos dos níveis do marcador N-acetil-aspartato/lactato, que tem sido associado a aumentos dos valores médios de morte celular e ao desenvolvimento de sequelas neurológicas em recém-nascidos afectados.Estes resultados promissores, juntamente com a sua maior biodisponibilidade e menor custo em comparação com o xénon, fazem do árgon uma molécula com um elevado potencial de tradução de banco-a-banco no tratamento do HIE.,conclusões alcançar um tratamento eficaz para a HIE é um dos grandes desafios que a medicina moderna enfrenta. Por esta razão, foram desenvolvidos esforços consideráveis durante anos para analisar os mecanismos que conduzem à lesão das células cerebrais após a asfixia perinatal, com o objectivo de desenvolver tratamentos eficazes para os bloquear. Actualmente, pediatras e neurocientistas estão a tentar desenvolver novos compostos que possam funcionar em sinergia com a hipotermia com o objectivo de reduzir ao mínimo as sequelas neurológicas do HIE., Por outro lado, estudos recentes têm começado a incluir o sexo entre as variáveis a ter em conta na gestão de HIE, como diforme diferenças sexuais foram encontrados tanto nos mecanismos de lesão (em modelos experimentais, as fêmeas apresentaram maiores déficits de memória, enquanto os machos mostraram uma maior susceptibilidade ao estresse oxidativo), e nos caminhos dos diferentes tratamentos em consideração., Apesar dos avanços promissores feitos com o uso de melatonina ou compostos como EPO, estudos pré-clínicos ainda são necessários para elucidar ainda mais os mecanismos de ação dessas moléculas, e ensaios clínicos com amostras maiores são necessários para determinar a dosagem ideal e as vias de administração destes e outros tratamentos.o estudo foi apoiado por uma subvenção concedida pela UPV/EHU no âmbito do programa de financiamento do grupo de investigação da Universidade (GIU 17/018).
conflitos de interesses
os autores não têm conflitos de interesses a declarar.