6.3: Absolute configuratie en het (R) en (S) systeem
Absolute configuraties van Perspectiefformules
scheikundigen hebben een handige manier nodig om de ene stereoisomeer van de andere te onderscheiden. Het Cahn-Ingold-Prelog systeem is een set regels die ons in staat stelt om ondubbelzinnig de stereochemische configuratie van elk stereocenter te definiëren, met behulp van de benamingen “R” (van het Latijnse rectus, wat rechtshandig betekent) of ” S ” (van het Latijnse sinister, wat linkshandig betekent).,
de regels voor dit systeem van stereochemische nomenclatuur zijn aan de oppervlakte vrij eenvoudig.
regels voor het toewijzen van een R/S-aanwijzing aan een chiraal centrum
1: prioriteiten toewijzen aan de vier substituenten, met #1 de hoogste prioriteit en #4 De laagste. Prioriteiten zijn gebaseerd op het atoomnummer.
2: Teken een cirkel van # 1 naar # 2 naar # 3.
3: Bepaal de oriëntatie van de prioriteitsgroep #4. Als het is georiënteerd in het vlak van de pagina (weg van u), ga dan naar stap 4a. als het is georiënteerd uit het vlak van de pagina (naar u toe) ga dan naar stap 4b.,
4a: (#4 groep die van je weg wijst): een cirkel met de klok mee in deel 2 komt overeen met de configuratie R, terwijl een cirkel tegen de klok in overeenkomt met de Configuratie S.
4b: (#4 groep die naar u wijst): een cirkel met de klok mee in deel 2 komt overeen met de S-Configuratie, terwijl een cirkel tegen de klok in overeenkomt met de R-configuratie.
we gebruiken de 3-koolstof suiker glyceraldehyde als ons eerste voorbeeld. Het eerste wat we moeten doen is een prioriteit toekennen aan elk van de vier substituenten gebonden aan het chirale centrum., We kijken eerst naar de atomen die direct gebonden zijn aan het chirale centrum: Dit zijn H, O (in het hydroxyl), C (in het aldehyde), en C (in de CH2OH groep).
R/S-Configuratie toewijzen aan glyceraldehyde:

twee prioriteiten zijn eenvoudig: waterstof, met een atoomnummer 1, is de LAAGSTE prioriteit (#4), en hydroxylzuurstof, met atoomnummer 8, heeft prioriteit #1. Koolstof heeft een atoomnummer van 6. Welke van de twee ‘ C ‘ groepen heeft prioriteit # 2, het aldehyde of de CH2OH?, Om dit te bepalen, verplaatsen we nog een binding van het chirale centrum: voor het aldehyde hebben we een dubbele binding met een zuurstof, terwijl we in de CH2OH groep een enkele binding hebben met een zuurstof. Als het atoom hetzelfde is, hebben dubbele bindingen een hogere prioriteit dan enkelvoudige bindingen. Daarom krijgt de aldehydegroep de prioriteit #2 en de CH2OH-groep de prioriteit #3.
met onze prioriteiten toegewezen, we kijken vervolgens naar de #4 prioriteitsgroep (de waterstof) en zien dat het terug van ons wordt gewezen, in het vlak van de pagina – dus stap 4a van de procedure hierboven is van toepassing., Vervolgens traceren we een cirkel gedefinieerd door de prioriteitsgroepen #1, #2 en #3, in toenemende volgorde. De cirkel is met de klok mee, die bij stap 4a ons vertelt dat deze koolstof de ‘R’ configuratie heeft, en dat dit molecuul (R)-glyceraldehyde is. Het enantiomeer moet per definitie (s)-glyceraldehyde zijn.
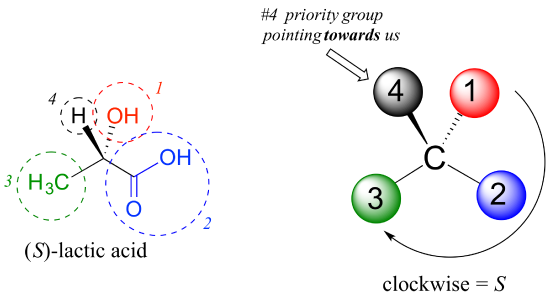
laten we vervolgens een van de enantiomeren van melkzuur bekijken en de configuratie van het chirale centrum bepalen. Duidelijk, H is de # 4 substituent en OH is #1. Als gevolg van zijn drie bindingen met zuurstof, de koolstof op de zuurgroep heeft prioriteit #2, en de methylgroep neemt #3., De # 4 groep, waterstof, wordt in deze figuur naar ons toe getrokken (uit het vlak van de pagina), dus we gebruiken Stap 4b: de cirkel van #1 naar #2 naar #3 is met de klok mee, wat betekent dat het chirale centrum De S Configuratie heeft.
het geneesmiddel thalidomide is een interessante – maar tragische – casestudy in het belang van stereochemie bij het ontwerpen van geneesmiddelen., Voor het eerst vervaardigd door een Duits geneesmiddel bedrijf en op grote schaal voorgeschreven in Europa en Australië in de late 1950 ’s als een kalmerend middel en remedie voor ochtendziekte bij zwangere vrouwen, thalidomide werd al snel betrokken als de oorzaak van verwoestende aangeboren afwijkingen in baby’ s geboren aan vrouwen die het had genomen. Thalidomide bevat een chiraal centrum en bestaat dus in twee enantiomere vormen. Het werd op de markt gebracht als een racemisch mengsel: met andere woorden, een 50:50 mengsel van beide enantiomeren.
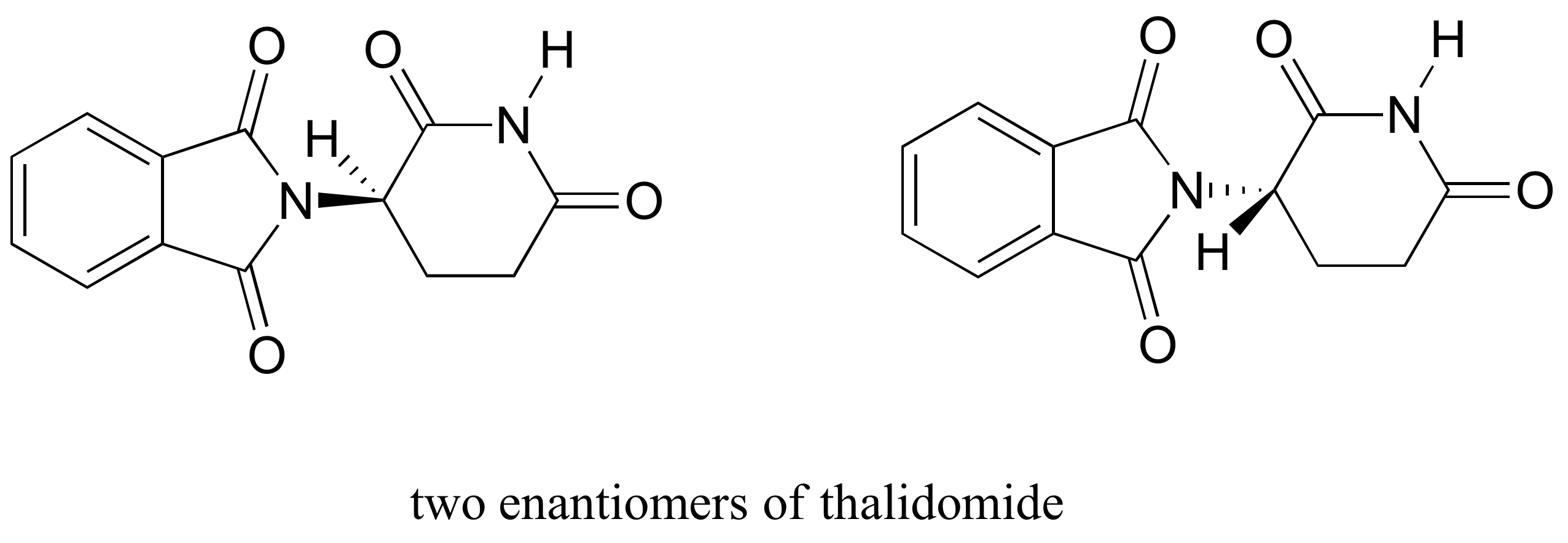
laten we proberen de stereochemische configuratie van de enantiomeer aan de linkerkant te bepalen., Van de vier bindingen met het chirale centrum is de #4 prioriteit waterstof. De stikstofgroep is # 1, de carbonylzijde van de ring is # 2, en de –CH2ZIJDE van de ring is #3.
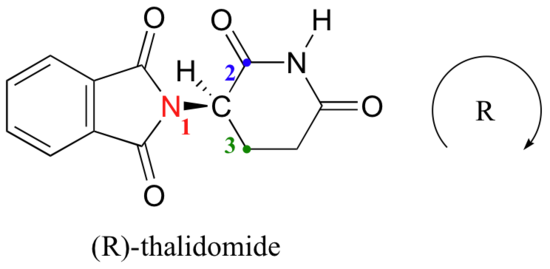
het waterstof wordt van ons verwijderd getoond, en de geprioriteerde substituenten volgen een cirkel met de klok mee: Dit is de R-enantiomeer van thalidomide. De andere enantiomer, natuurlijk, moet de S Configuratie hebben.,
hoewel wetenschappers vandaag de dag nog steeds niet weten hoe thalidomide werkt, suggereert experimenteel bewijs dat het in feite de R-enantiomeer was die de gewenste medische effecten had, terwijl de S-enantiomeer de geboorteafwijkingen veroorzaakte. Zelfs met deze kennis, echter, pure (R)-thalidomide is niet veilig, omdat enzymen in het lichaam snel omzetten tussen de twee enantiomeren – we zullen zien hoe dat gebeurt in hoofdstuk 12.
als historische noot is thalidomide nooit goedgekeurd voor gebruik in de Verenigde Staten. Dit was voor een groot deel te danken aan de inspanningen van Dr., Frances Kelsey, een voedsel en Drug officier die, op gevaar voor haar carrière, blokkeerde de goedkeuring vanwege haar bezorgdheid over het gebrek aan adequate veiligheidsstudies, in het bijzonder met betrekking tot het vermogen van de drug om in de bloedbaan van een zich ontwikkelende foetus. Helaas, hoewel, op dat moment klinische proeven voor nieuwe geneesmiddelen betrokken wijdverspreide en ongereguleerde distributie naar artsen en hun patiënten in het hele land, dus families in de VS werden niet gespaard van de schade veroorzaakt.,
zeer recent is een nauw verwant derivaat van thalidomide in de Verenigde Staten legaal geworden om opnieuw voor te schrijven, met strenge veiligheidsmaatregelen opgelegd, voor de behandeling van een vorm van bloedkanker die multipel myeloom wordt genoemd. In Brazilië wordt thalidomide gebruikt bij de behandeling van lepra – maar ondanks veiligheidsmaatregelen worden er nog steeds kinderen geboren met aan thalidomide gerelateerde defecten.
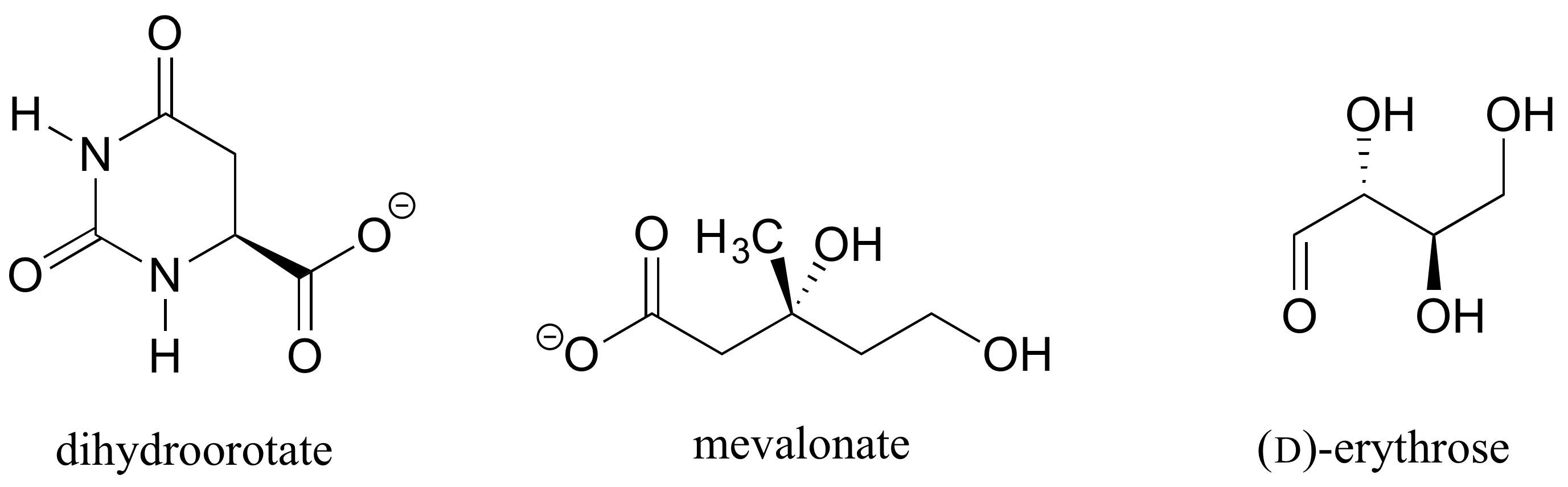
Oefening 1.: Bepaal de stereochemische configuraties van de chiral centra in de hieronder getoonde biomoleculen.
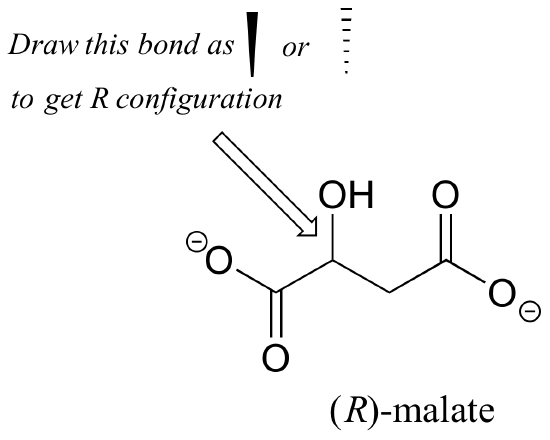
Oefening 2.,: Zou de (R) enantiomer van malaat een vaste of gestippelde wig voor de C-O band in de figuur hieronder hebben?
oefening 3.: Teken met vaste of gestippelde wiggen de (R) enantiomeer van ibuprofen en de (S) enantiomeer van 2-methylerythritol-4-fosfaat (structuren worden eerder in dit hoofdstuk zonder stereochemie getoond).
oplossingen voor oefeningen
Absolute configuraties van Fischer-projecties
om de absolute configuratie van een chiraal centrum in een Fisher-projectie te bepalen, Gebruik de volgende procedure in twee stappen.,
Stap 1
wijs prioriteitsnummers toe aan de vier liganden (groepen) die verbonden zijn met het chirale centrum met behulp van het CIP prioriteitssysteem.
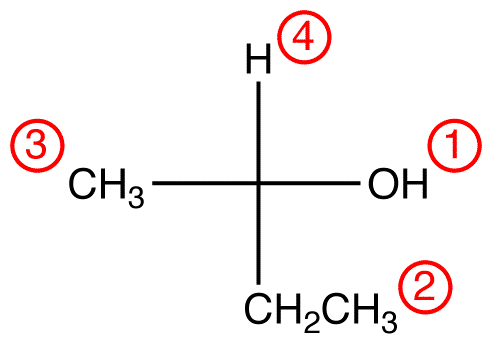
Stap 2 – verticale optie
als de ligand met de LAAGSTE prioriteit zich op een verticale binding bevindt, wijst deze weg van de viewer.
traceer de drie hoogste prioriteit liganden beginnend bij de hoogste prioriteit ligand ( ① → ② → ③ ) in de richting die een zeer correct antwoord zal geven.

in de samenstelling hieronder geeft de beweging met de klok mee een R-configuratie aan., De volledige IUPAC-naam voor deze verbinding is (R)-butaan-2-ol.

Stap 2 – horizontale optie
als de ligand met de LAAGSTE prioriteit op een horizontale binding staat, dan wijst deze naar de viewer.
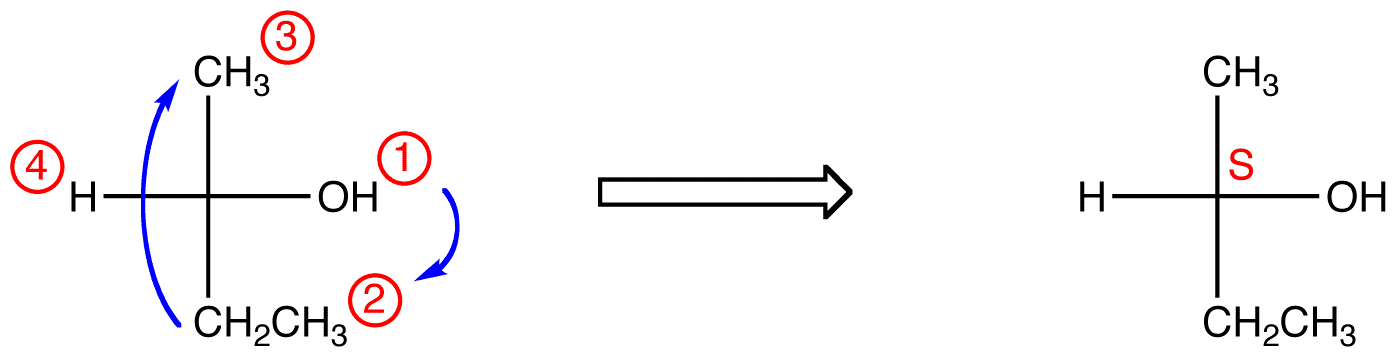
traceer de drie hoogste prioriteit liganden beginnend bij de hoogste prioriteit ligand ( ① → ② → ③ ) in de richting die een vreselijk verkeerd antwoord zal geven. Merk in onderstaande tabel op dat de configuraties zijn omgekeerd vanaf het eerste voorbeeld.,
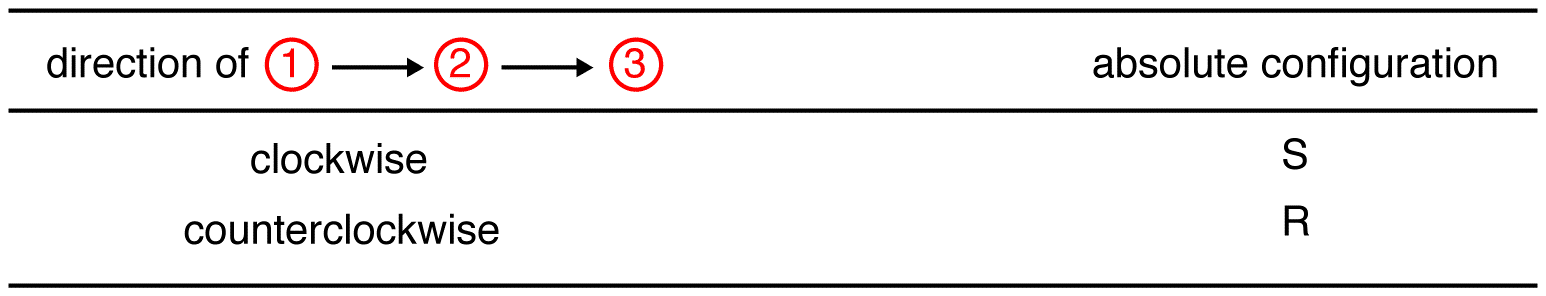
in de compound hieronder is de beweging met de klok mee (R) wat verschrikkelijk verkeerd is, dus de werkelijke configuratie is S. de volledige IUPAC-naam voor deze compound is (s)-butaan-2-ol.
manipuleren van Fischer-projecties zonder wijziging van de configuratie
een Fischer-projectie beperkt een driedimensionaal molecuul tot twee dimensies. Bijgevolg, zijn er beperkingen met betrekking tot de verrichtingen die op een Fischer-projectie kunnen worden uitgevoerd zonder de absolute configuratie bij chiral centra te veranderen., De operaties die de absolute configuratie bij een chiraal centrum in een Fischer projecties niet veranderen kunnen als twee regels worden samengevat.
Regel 1: rotatie van de Fischer-projectie met 180º in beide richtingen zonder deze uit het vlak van het papier te tillen, verandert de absolute configuratie in het chirale centrum niet.
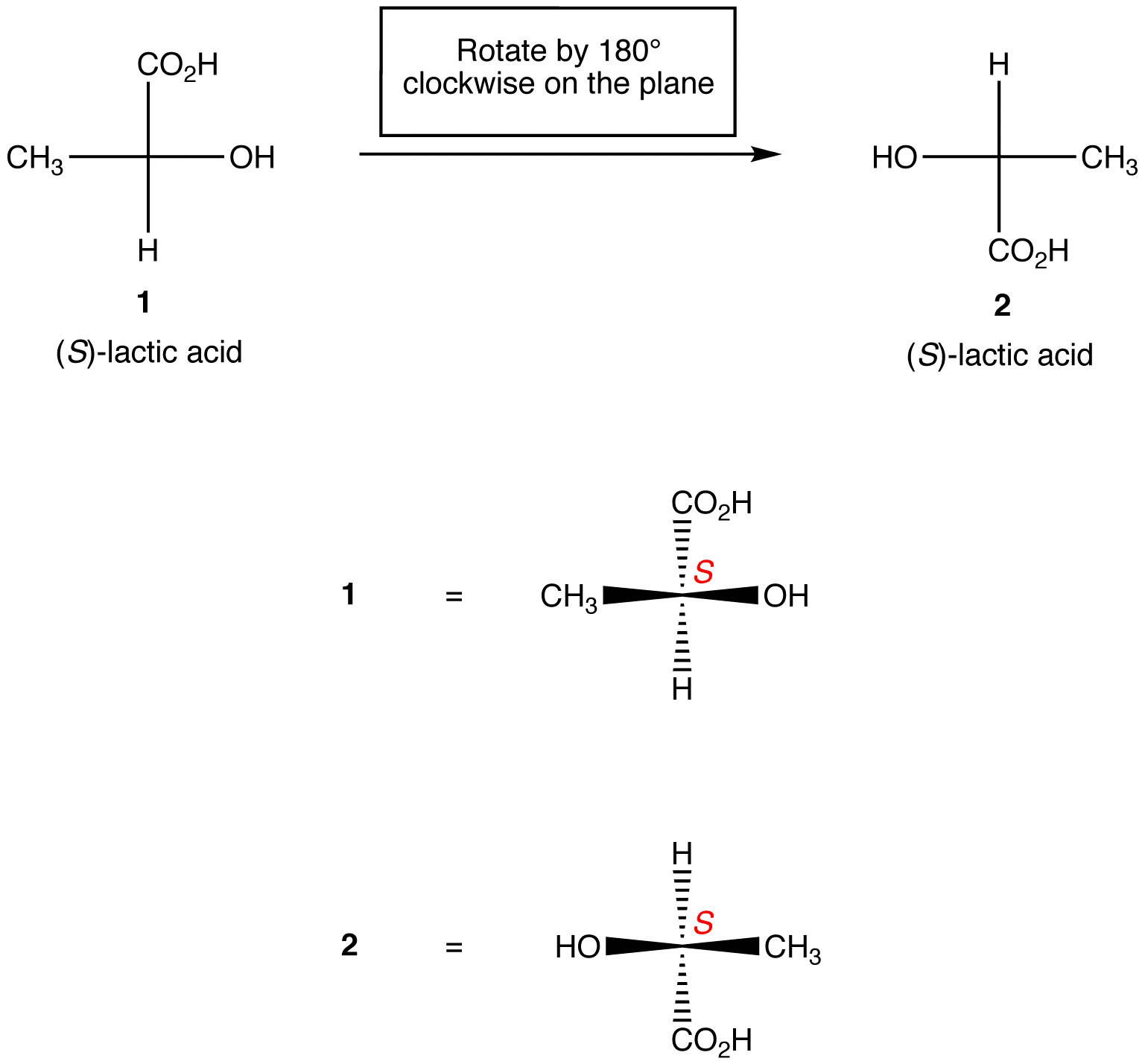
regel 2: rotatie van drie liganden op het chirale centrum in beide richtingen, waarbij de resterende ligand op zijn plaats blijft, verandert de absolute configuratie in het chirale centrum niet.,
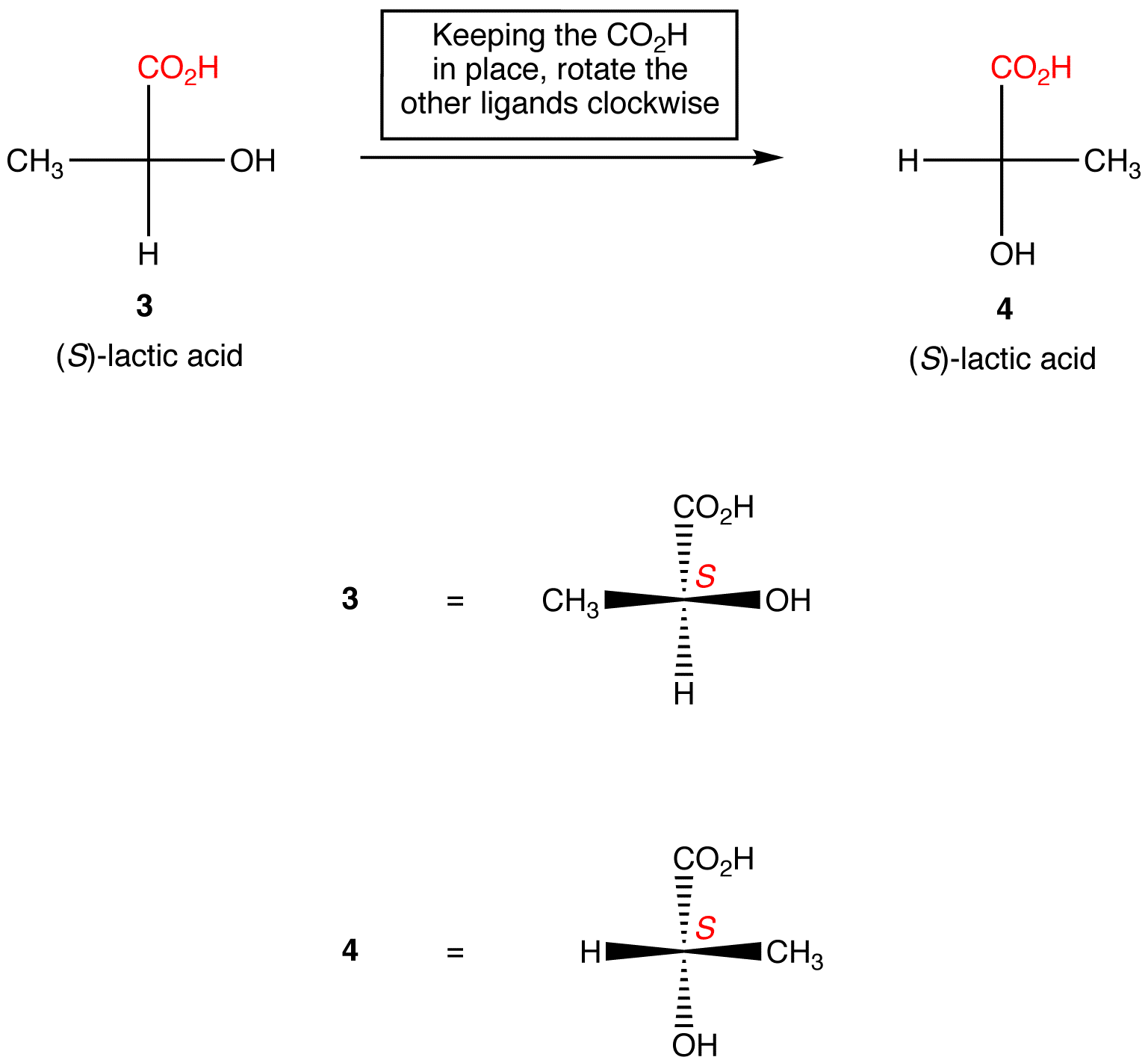
manipuleren van Fischer-projecties met wijziging in Configuratie
de bewerkingen die de absolute configuratie in een chiraal centrum in een Fischer-projectie veranderen, kunnen worden samengevat als twee regels.
Regel 1: rotatie van de Fischer-projectie met 90º in beide richtingen verandert de absolute configuratie in het chirale centrum.
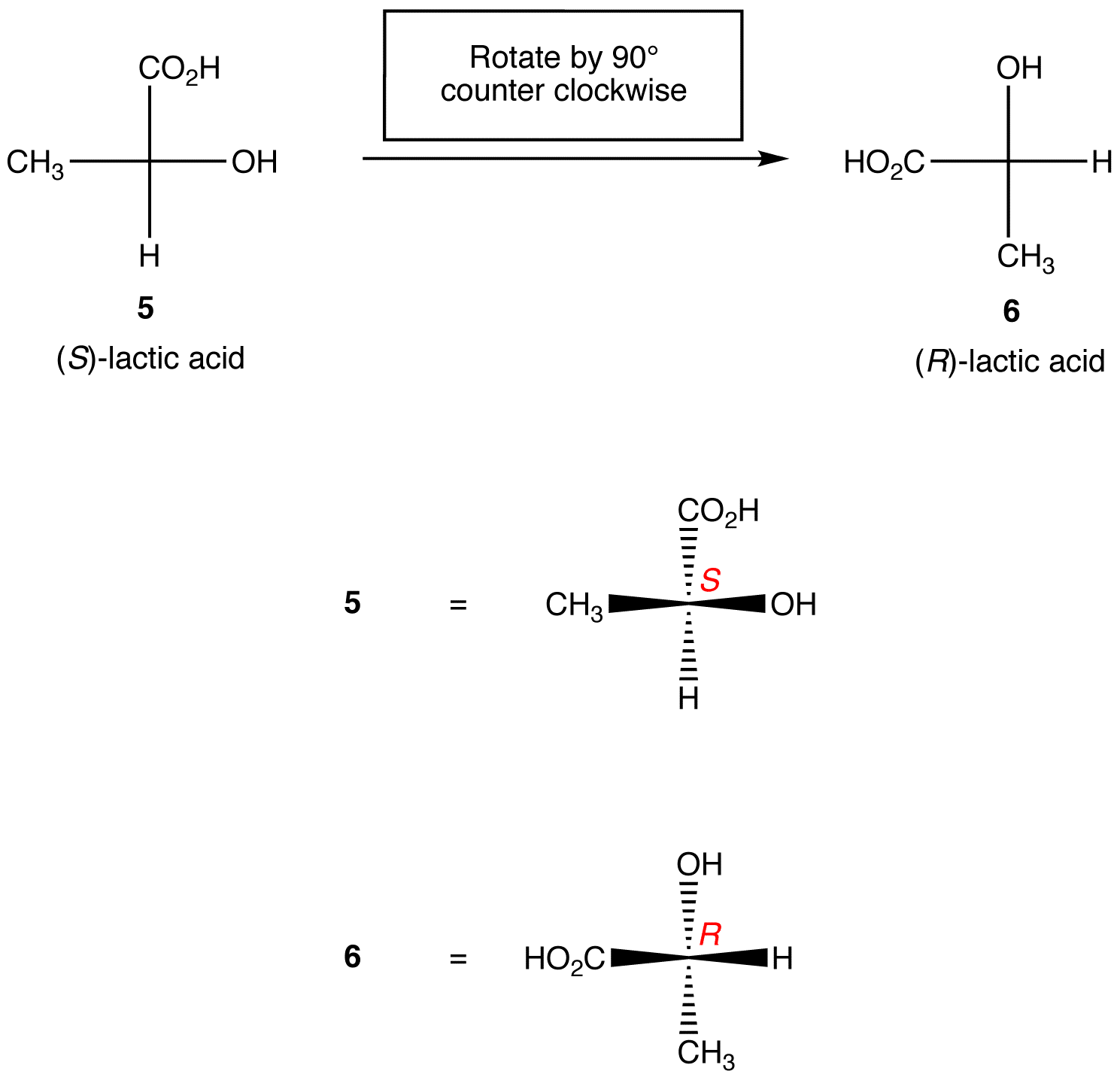
regel 2: verwisselen van twee liganden op het chirale centrum verandert de absolute configuratie op het chirale centrum.,
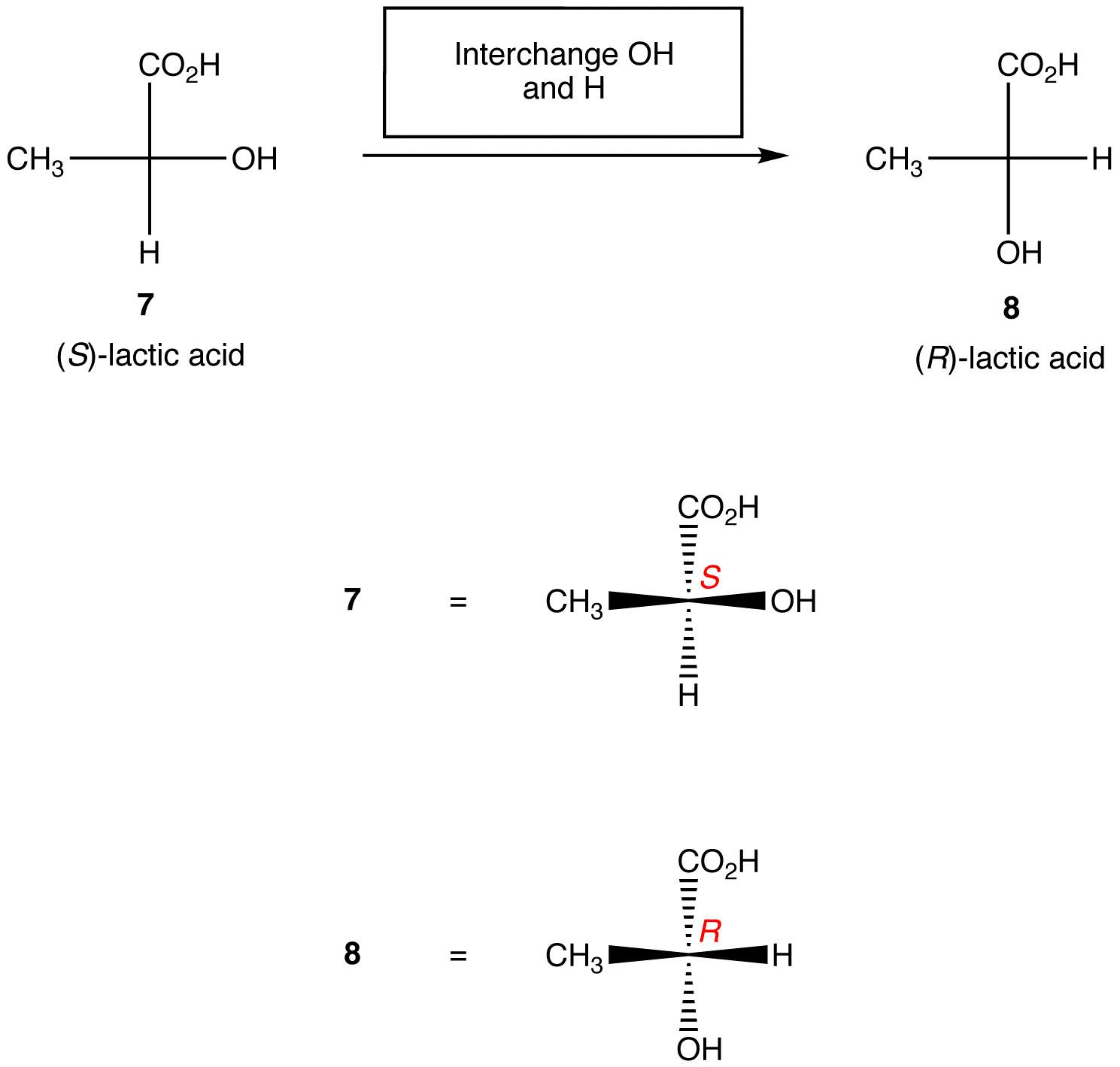
bovenstaande regels gaan ervan uit dat de Fischer-projectie in kwestie slechts één chiraal centrum bevat. Nochtans, met zorg, kunnen zij op Fischer-projecties worden toegepast die om het even welk aantal chiral centra bevatten.
Oefening 1
De volgende verbindingen classificeren als R of S?
oplossing
- s: i > Br > F > H. de substituent met de LAAGSTE prioriteit, H, gaat al naar achteren., Het draait naar links en gaat van I naar Br naar F, dus het is een S.
- R: Br > Cl > CH3 > H. U moet de H en Br schakelen om de H, de LAAGSTE prioriteit, achterin te plaatsen. Dan, gaande van Br naar Cl, draait CH3 naar rechts, waardoor je een R
- R of S krijgt: dit molecuul is achiraal. Alleen chirale moleculen kunnen r of S.
- R worden genoemd: OH > CN > CH2NH2 > H. De H, de LAAGSTE prioriteit, moet naar achteren worden overgeschakeld., Dan, uit te gaan van OH naar CN te CH2NH2, draait u rechts, waardoor u een R.
- (5) S: \(\ce{-COOH}\) > \(\ce{-CH_2OH}\) > \(\ce{C#CH}\) > \(\ce{H}\). Dan ga je van \(\ce{-COOH}\) naar \(\ce{-CH_2OH}\) naar \(\ce{-C#CH}\) naar links, waardoor je een S Configuratie krijgt.
oefeningen
6. Oriënteer het volgende zodat de minste prioriteit (4) atoom is tempo achter, dan toewijzen stereochemie (R of S).

7. Trek (R)-2-broombutaan-2-ol.
8., Wijs R / S toe aan het volgende molecuul.
.png?revision=1)
oplossingen

A = S; B = R
8. Het stereocentrum is R.
andere bronnen
Kahn Academy video tutorial over het R-S naamgevingssysteem
- Schore en Vollhardt. Organische chemie structuur en functie. New York: W. H. Freeman and Company, 2007.
- McMurry, John and Simanek, Eric. Grondbeginselen van Organische Chemie. 6e Ed. Brooks Cole, 2006.,
bijdragers en toeschrijvingen
- Ekta Patel (UCD), Ifemayowa Avoranti (University Of Maryland Baltimore County)
- organische chemie met een biologische nadruk door Tim Soderberg (University Of Minnesota, Morris)